Medicinsk validering og kliniske standarder for AI-blodprøveanalyse
Triple-blind klinisk valideringsmetode, tilsyn af bestyrelsescertificerede læger og korrelationsstudier af resultater i den virkelige verden, der driver verdens mest betroede AI blodprøveanalysator.
Primær bevismateriale og dokumentation
Påstandene og valideringsdataene, der præsenteres på denne side, er dokumenteret i vores tekniske rapport (fagfællebedømmelse afventer). Se den fulde metode og den understøttende dokumentation nedenfor.
Klinisk valideringsramme for AI-drevet blodprøvefortolkning
Triple-blind valideringsmetode, præstationsmålinger og kvalitetssikringsprotokoller
Klinisk valideringsramme
Kantestis AI-blodprøvefortolkning Platformen gennemgår streng medicinsk validering for at sikre klinisk pålidelighed. Vores flerlagsvalideringsproces kombinerer maskinlæringsvalidering med traditionelle kliniske gennemgangsmetoder.
Hver algoritmeopdatering gennemgår en triple-blind klinisk validering, før den når produktion. Denne side dokumenterer vores komplette valideringsramme, lægetilsynsstruktur og løbende kvalitetsovervågningsprotokoller.
Triple-blind klinisk valideringsproces
Vores valideringsmetode eliminerer bekræftelsesbias gennem en uafhængig gennemgangsproces i tre trin. Hvert trin fungerer uden kendskab til de andres konklusioner, hvilket sikrer objektiv nøjagtighedsmåling.
AI-fortolkning
AI-systemet analyserer blodprøveresultater uden adgang til klinisk diagnose, patienthistorik eller lægejournaler. Denne blinde analyse sikrer, at AI'ens fortolkning udelukkende er baseret på biomarkørdata og etablerede referenceområder.
- Ingen adgang til klinisk diagnose
- Populationsjusterede referenceintervaller
- Multiparameter korrelationsanalyse
Lægeanmeldelse
Bestyrelsescertificerede patologer gennemgår uafhængigt de samme blodprøveresultater. Læger har ikke adgang til AI-fortolkninger, hvilket sikrer, at deres kliniske vurdering forbliver upartisk.
- Bestyrelsescertificerede kliniske patologer
- Ingen synlighed af AI-output
- Standardiserede gennemgangsprotokoller
Uafhængig sammenligning
Et tredjeparts klinisk team sammenligner AI-output med lægernes konsensus uden at vide, hvilken fortolkning der stammer fra hvilken kilde. Uoverensstemmelser udløser yderligere gennemgangscyklusser.
- Blind sammenligningsmetode
- Statistisk konkordansanalyse
- Fuld dokumentation af revisionsspor
Triple-blind valideringsworkflow
Vores valideringsproces sikrer upartisk nøjagtighedsvurdering gennem uafhængige parallelle evalueringsstrømme, der kun konvergerer ved den endelige sammenligning.
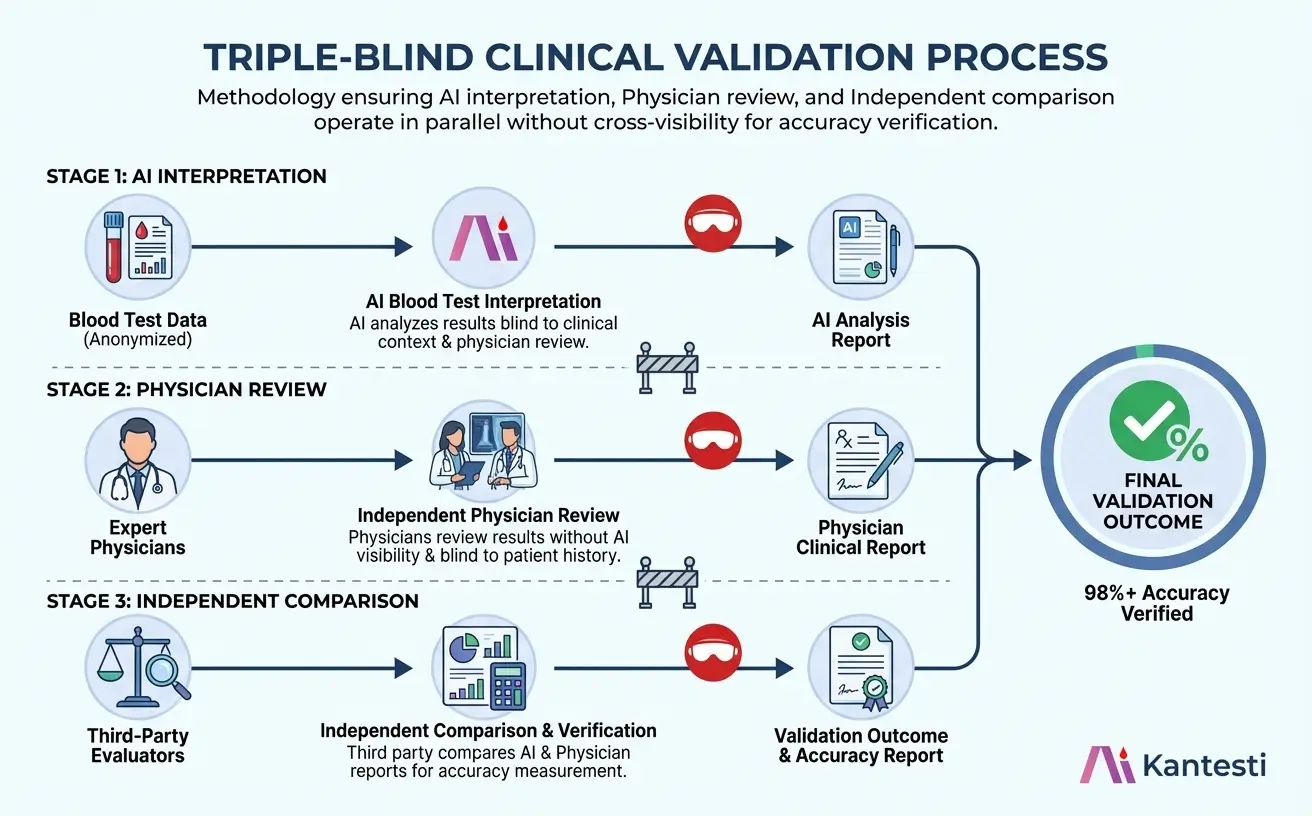
Triple-blind valideringsmetode: AI-fortolkning (fase 1), lægegennemgang (fase 2) og uafhængig sammenligning (fase 3) fungerer parallelt uden krydssynlighed.
Valideret ydeevne efter testkategori
Præstationsmålinger valideret gennem triple-blind klinisk gennemgang på tværs af mere end 1.000.000 testtilfælde. Resultaterne viser ensartet nøjagtighed på tværs af alle større biomarkørkategorier.
Oversigt over samlet nøjagtighed
Samlet nøjagtighed: 98,7% — Vægtet gennemsnit på tværs af alle testkategorier baseret på triple-blind lægekonkordans. Individuelle kategoriers præstation varierer fra 98,1% til 99,3% sensitivitet. Se rapport §4.1, tabel 2
Korrelation mellem kliniske resultater: 87% — Longitudinel korrelation med bekræftede diagnoser i opfølgningsstudier i den virkelige verden. Se rapport §4.3
| Testkategori | Følsomhed | Specificitet | Prøvestørrelse |
|---|---|---|---|
| Komplet blodtælling (CBC) | 99.3% | 99.0% | 285,000 |
| Omfattende metabolisk panel | 99.1% | 98.9% | 198,000 |
| Lipidpanel | 98.8% | 98.5% | 167,000 |
| Skjoldbruskkirtelfunktion | 98.4% | 98.1% | 142,000 |
| Leverfunktionstests | 98.9% | 98.6% | 124,000 |
| Nyrefunktionspanel | 99.2% | 99.0% | 84,000 |
Befolkningskonsistens
Valideringsresultaterne viser ensartethed i 99%-nøjagtigheden på tværs af alle demografiske grupper uanset etnicitet, alder, køn eller geografisk region. Befolkningsproportional stikprøveudtagning sikrer repræsentativ dækning på tværs af 197 lande.
Global valideringsdatasætdistribution
Vores træningsdatasæt på 15 millioner prøver og over 1 million valideringssager er fordelt på tværs af alle større globale regioner for at sikre en nøjagtig, populationsrepræsentativ analyse.
Medicinsk Rådgivende Udvalg
Vores medicinske rådgivende udvalg yder klinisk tilsyn med al udvikling og validering af AI-algoritmer. Bestyrelsesmedlemmerne repræsenterer forskellige specialer på tværs af flere lande og bringer samlet set mere end 180 års ekspertise inden for klinisk medicin.
Thomas Klein, læge
Cheflæge (CMO) Klinisk hæmatologi og AI-diagnostikDr. Sarah Mitchell, læge, ph.d.
Chefmedicinsk rådgiver Klinisk patologi og laboratoriemedicinProfessor Dr. Hans Weber
Senior lægefaglig rådgiver Laboratoriemedicin og klinisk kemiDr. Maria Rodriguez, læge, MPH
Medicinsk rådgiver Intern medicin og forebyggende medicinDr. Chen Wei, læge, kandidatgrad
Medicinsk rådgiver Endokrinologi og metabolisk medicinMød vores komplette medicinske rådgivende udvalg med detaljerede profiler, kvalifikationer og forskningsbaggrund.
Se alle rådgivere →Løbende kvalitetsovervågning
Validering efter implementering fortsætter gennem strukturerede overvågningsprotokoller. Ydeevne i den virkelige verden spores i forhold til kliniske resultater, med feedback-loops, der muliggør løbende forbedringer.
Månedlige præstationsrapporter
Omfattende nøjagtighedsanalyse på tværs af alle biomarkørkategorier, demografiske segmenter og geografiske regioner. Trendidentifikation muliggør proaktiv kvalitetsstyring.
Interlaboratoriekonkordans
Testning på tværs af mere end 500 laboratoriesystemer validerer ensartet ydeevne uanset udstyrsproducent, metode eller kalibreringsstandarder.
Kliniske resultatstudier
Longitudinelle korrelationsstudier sporer AI-fortolkninger i forhold til bekræftede diagnoser og opnår 87%-korrelation med kliniske resultater på tværs af forskellige patientpopulationer.
Feedback fra sundhedsudbydere
Struktureret feedbackintegration fra læger og laboratoriepersonale. Markerede fortolkninger gennemgås af det medicinske rådgivende udvalg, og rettelser integreres i træningen.
Træningsdata og kvalitetssikring
Vores AI-model er trænet på et af de største kuraterede blodprøvedatasæt i branchen, med strenge kvalitetskontroller, der sikrer dataintegritet og klinisk relevans.
Datasætets sammensætning
- Samlede prøver15 millioner
- Geografisk dækning197 lande
- Laboratoriekilder500+ certificerede laboratorier
- Datointerval2015-2025
- Biomarkørtyper450+ parametre
Kvalitetskontroller
Flertrins datakvalitetssikring:
- Kun ISO 15189-certificerede laboratoriekilder
- Fjernelse af ufuldstændige eller beskadigede optegnelser
- Outlier-detektion for præanalytiske fejl
- Proveniensverifikation for alle datasæt
- HIPAA/GDPR-kompatibel anonymisering
Teknologi- og compliance-partnere
Vores valideringsinfrastruktur og AI-udvikling understøttes gennem partnerskaber med brancheførende teknologiudbydere.
Microsoft FoundersHub
Cloud-infrastruktur og AI-udviklingsplatform i virksomhedsklassen, der understøtter skalerbare valideringsworkflows.
NVIDIA Inception Program
GPU-beregningsressourcer og AI-modeloptimering muliggør effektiv træning på over 15 millioner eksempeldatasæt.
Google Cloud AI
Maskinlæringsinfrastruktur, der understøtter distribueret modeltræning og inferens i realtid.
Cloudflare
Globalt edgenetværk, der sikrer sikker adgang med lav latenstid på tværs af 197 lande.
SOC 2 Type II-kontroller
Sikkerhedskontroller i overensstemmelse med AICPA-standarder
ISO 27001-tilpasset
Styringskontroller for informationssikkerhed
HIPAA-tilpassede kontroller
Databeskyttelsesforanstaltninger inden for sundhedsvæsenet i USA
GDPR-kompatibel
Den europæiske databeskyttelsesforordning
Korrekt brug og begrænsninger
Gennemsigtighed omkring muligheder og begrænsninger er afgørende for ansvarlig implementering af AI i sundhedsvæsenet. Kantesti er udviklet som et beslutningsstøtteværktøj, der skal supplere – ikke erstatte – professionel medicinsk vurdering.
Oplysninger ikke tilgået
Vores AI fortolker biomarkørdata isoleret. Følgende kliniske kontekst er ikke tilgængelig for systemet:
- Komplet patientens sygehistorie
- Nuværende medicin og potentielle interaktioner
- Resultater af fysisk undersøgelse
- Genetiske faktorer og familiehistorie
- Livsstilsfaktorer (medmindre brugeren har angivet dem)
Variationer i laboratoriemetodologi
Referenceområderne varierer mellem laboratorier på grund af forskelle i udstyr og kalibreringsstandarder. Vores database med over 45.000 laboratoriespecifikke områder dækker de fleste variationer, men brugerne bør kontrollere, at de udtrukne værdier stemmer overens med deres oprindelige rapport.
Overvejelser vedrørende dokumentkvalitet
OCR-nøjagtigheden afhænger af dokumentkvaliteten. Håndskrevne resultater eller scanninger med lav opløsning kan påvirke værdiudtrækningen. Manuel korrektion er tilgængelig for alle udtrukne værdier før analyse.
Medicinsk ansvarsfraskrivelse
Kantesti er et AI-drevet informationsværktøj, der fortolker blodprøveresultater baseret på etablerede medicinske referenceområder og kliniske retningslinjer. Det er IKKE en medicinsk enhed og diagnosticerer, behandler, helbreder eller forebygger ikke nogen sygdom.
Oplysningerne er kun til uddannelsesmæssige og informative formål og bør ikke betragtes som lægefaglig rådgivning. Rådfør dig altid med en kvalificeret sundhedsperson, før du træffer beslutninger om dit helbred eller din behandling.
I tilfælde af medicinske nødsituationer skal du straks kontakte nødtjenesterne. Kantesti er ikke beregnet til nødsituationer.
Interessekonflikter og finansieringsoplysninger
Denne valideringsdokumentation er udgivet af Kantesti/PIYA AI. Medlemmer af det medicinske rådgivende udvalg modtager kompensation for deres rådgivende roller. CMO'en (Thomas Klein, MD) er fuldtidsansat hos Kantesti AI. Alle valideringsdata er blevet uafhængigt verificeret via triple-blind metode. Der blev ikke modtaget ekstern finansiering til valideringsstudier. Virksomheden er selvfinansieret gennem indtægts- og teknologipartnerskaber med Microsoft, NVIDIA, Google Cloud og Cloudflare.
Ofte stillede spørgsmål om medicinsk validering
Hvad betyder "triple-blind validering"?
Triple-blind validering betyder, at tre uafhængige parter analyserer de samme data uden at kende hinandens konklusioner. Vores AI fortolker blodprøver uden klinisk kontekst, læger gennemgår dem uafhængigt uden at se AI-output, og et tredje team sammenligner resultaterne uden at vide, hvilke der kommer fra AI vs. læger. Dette eliminerer bekræftelsesbias og sikrer objektiv nøjagtighed i målingen.
Hvor ofte opdateres AI-modellen?
Vores model gennemgår kvartalsvis genoptræning, der inkorporerer nye validerede data, opdaterede kliniske retningslinjer og ny biomarkørforskning. Hver opdatering gennemgår den fulde triple-blinde valideringsprotokol før implementering. Opdateringer, der ikke opfylder vores nøjagtighedsgrænse, afvises.
Hvorfor varierer nøjagtigheden afhængigt af testkategori?
Nogle biomarkører har mere standardiserede referenceområder globalt (som elektrolytter), mens andre varierer mere mellem laboratorier og populationer (som skjoldbruskkirtelhormoner). Kategorier med mere variation viser en smule lavere nøjagtighed på grund af den iboende kompleksitet i fortolkningen.
Kan jeg stole på AI-fortolkning af medicinske beslutninger?
Kantesti er designet som et beslutningsstøtteværktøj, ikke en erstatning for professionel medicinsk vurdering. Vores AI leverer validerede fortolkninger baseret på etablerede referenceområder, men klinisk kontekst - herunder din sygehistorie, medicin og symptomer - kræver lægeevaluering for behandlingsbeslutninger. Rådfør dig altid med din læge.
Hvordan håndteres populationsdiversitet i validering?
Vores træningsdata omfatter 15 millioner stikprøver proportionalt fordelt på tværs af 197 lande, hvor populationsvægtet stikprøveudtagning sikrer repræsentation fra alle større etniske og geografiske grupper. Kvartalsvise retfærdighedsrevisioner verificerer nøjagtighed og konsistens på tværs af demografiske grupper, hvor 99%-konsistens opretholdes på tværs af alle befolkningssegmenter.
Hvad sker der, hvis AI'en laver en fejl?
Sundhedsudbydere og brugere kan markere fortolkninger til gennemgang af det medicinske rådgivende udvalg. Markerede tilfælde analyseres af vores CMO, Thomas Klein, MD, og det medicinske team. Hvis fejl bekræftes, integreres rettelser i fremtidige træningscyklusser. Vores løbende overvågning sporer den praktiske præstation for at identificere og adressere systematiske problemer proaktivt.
Hvor kan jeg finde den fulde valideringsrapport?
Vores komplette valideringsmetode er dokumenteret i den tekniske rapport "Clinical Validation Framework for AI-Powered Blood Test Interpretation" (Rapport-ID: KANTESTI-TR-2025-001, DOI: 10.5281/kantesti.2025.mv2). Den fulde rapport er tilgængelig via DOI-linket, på ResearchGate og som en PDF-fil, der kan downloades fra vores hjemmeside.
Hvem anmelder det medicinske indhold på Kantesti?
Alt medicinsk indhold er skrevet og gennemgået af Thomas Klein, MD, vores ledende læge. Dr. Klein er en bestyrelsescertificeret klinisk hæmatolog tilknyttet Istanbul Nisantasi Universitets Institut for Hæmatologi med over 15 års erfaring inden for laboratoriemedicin og AI-assisteret diagnostik. Yderligere tilsyn ydes af vores 12-medlem store medicinske rådgivende udvalg.
Erfaringsvalideret AI-blodprøveanalyse
Slut dig til millioner af brugere verden over, der stoler på Kantestis AI-blodprøveanalysator til klinisk valideret blodprøvefortolkning på over 75 sprog.
Virksomhedens gennemsigtighed
Vi tror på fuld gennemsigtighed omkring, hvem vi er, og hvordan vi opererer. Nedenfor finder du vores virksomhedsregistreringsoplysninger og information om ledelse.
Kantesti AI - PIYA AI
Juridisk enhed: PIYA AI (Kantesti Brand Owner)
Virksomhedstype: AI-sundhedsteknologi
Grundlagt: 2019
Hovedkvarter: Köln, Tyskland
Kontakte: [email protected]
Telefon: +49 177 497 4039
Ledelse
Grundlægger og administrerende direktør: Julian Emirhan Bulut
Visionær iværksætter, der leder AI-innovation inden for sundhedsteknologi. Udvikler tilgængelige værktøjer til fortolkning af blodprøver til forbedring af global sundhed.
Opret forbindelse på LinkedInLedende læge: Thomas Klein, læge
Bestyrelsescertificeret klinisk hæmatolog, der leder medicinsk validering og klinisk supervision.
Overholdelse og certificeringer
Databeskyttelse: GDPR-kompatibel (EU)
Sundhedsbeskyttelse: HIPAA-tilpassede sikkerhedsforanstaltninger (USA)
Sikkerhed: SOC 2 Type II-kontroller
Kvalitetsstyring: ISO 27001-tilpasset
Medicinsk udstyr: Ikke klassificeret som medicinsk udstyr - Kun et informationsværktøj
Referencer og standarder
Vores valideringsmetode og kliniske standarder er baseret på etablerede medicinske retningslinjer og internationale standarder.
- [1] Verdenssundhedsorganisationen (WHO). Brug af glykeret hæmoglobin (HbA1c) til diagnosticering af diabetes mellitus. Genève: WHO; 2011. Tilgængelig fra: https://www.who.int/diabetes/publications/diagnosis_diabetes2011/en/
- [2] International Standardiseringsorganisation. ISO 15189:2022 Medicinske laboratorier — Krav til kvalitet og kompetence. Genève: ISO; 2022. https://www.iso.org/standard/76677.html
- [3] Institut for Kliniske og Laboratoriestandarder (CLSI). EP09c: Sammenligning af måleprocedurer og biasestimering ved hjælp af patientprøver. 3. udg. Wayne, PA: CLSI; 2018.
- [4] Nationale Sundhedsinstitutter (NIH). Referenceområder for blodprøver. Bethesda, MD: NIH; Opdateret 2024. Tilgængelig fra: MedlinePlus
- [5] Amerikansk forening for klinisk kemi (AACC). Referenceområder for laboratorietest. Washington, DC: AACC; 2024. https://www.aacc.org/
- [6] Den Internationale Føderation for Klinisk Kemi (IFCC). Referencemålingsprocedurer. Milano: IFCC; 2023. https://www.ifcc.org/
- [7] Klein T. Klinisk valideringsramme for AI-drevet blodprøvefortolkning: Triple-blind valideringsmetode, præstationsmålinger og kvalitetssikringsprotokoller. Teknisk rapport KANTESTI-TR-2025-001, Version 2.0. Kantesti AI; 2025. DOI: 10.5281/kantesti.2025.mv2
- [8] Det amerikanske ministerium for sundhed og menneskelige tjenester. HIPAA-privatlivsregel. 45 CFR del 160 og underafsnit A og E af del 164. Washington, DC: HHS; 2013.
- [9] Europa-Parlamentet og Rådet. Den generelle forordning om databeskyttelse (GDPR). Forordning (EU) 2016/679. Bruxelles: EU; 2016.