Medicinsk validering och kliniska standarder för AI blodprovsanalys
Trippelblind klinisk valideringsmetodik, övervakning av läkarlegitimerade läkare och korrelationsstudier av verkliga resultat som driver världens mest betrodda AI blodprovsanalysator.
Primärbevis och dokumentation
Påståendena och valideringsdatan som presenteras på denna sida finns dokumenterade i vår tekniska rapport (peer review väntar). Se hela metoden och stödjande bevis nedan.
Klinisk valideringsramverk för AI-driven blodprovstolkning
Trippelblind valideringsmetodik, prestationsmått och kvalitetssäkringsprotokoll
Klinisk valideringsramverk
Kantestis Tolkning av AI-blodprov Plattformen genomgår rigorös medicinsk validering för att säkerställa klinisk tillförlitlighet. Vår flerstegsvalideringsprocess kombinerar maskininlärningsvalidering med traditionella kliniska granskningsmetoder.
Varje algoritmuppdatering genomgår trippelblind klinisk validering innan den når produktionsstart. Den här sidan dokumenterar vårt kompletta valideringsramverk, vår struktur för läkarövervakning och våra protokoll för kontinuerlig kvalitetsövervakning.
Trippelblind klinisk valideringsprocess
Vår valideringsmetodik eliminerar bekräftelsebias genom en oberoende granskningsprocess i tre steg. Varje steg fungerar utan kännedom om de andras slutsatser, vilket säkerställer objektiv noggrannhetsmätning.
AI-tolkning
AI-systemet analyserar blodprovsresultat utan tillgång till klinisk diagnos, patienthistorik eller läkarjournaler. Denna blinda analys säkerställer att AI:ns tolkning enbart baseras på biomarkördata och etablerade referensintervall.
- Ingen tillgång till klinisk diagnos
- Populationsjusterade referensintervall
- Korrelationsanalys med flera parametrar
Läkargranskning
Patologer med behörighet granskar samma blodprovresultat oberoende av varandra. Läkare har inte tillgång till AI-tolkningar, vilket säkerställer att deras kliniska bedömning förblir opartisk.
- Styrelsecertifierade kliniska patologer
- Ingen insyn i AI-utdata
- Standardiserade granskningsprotokoll
Oberoende jämförelse
Ett kliniskt team från tredje part jämför AI-resultat med läkarnas konsensus utan att veta vilken tolkning som kommer från vilken källa. Avvikelser utlöser ytterligare granskningscykler.
- Blind jämförelsemetodik
- Statistisk konkordansanalys
- Fullständig dokumentation av revisionsspår
Trippelblind valideringsarbetsflöde
Vår valideringsprocess säkerställer opartisk noggrannhetsbedömning genom oberoende parallella granskningsflöden som konvergerar endast vid den slutliga jämförelsen.
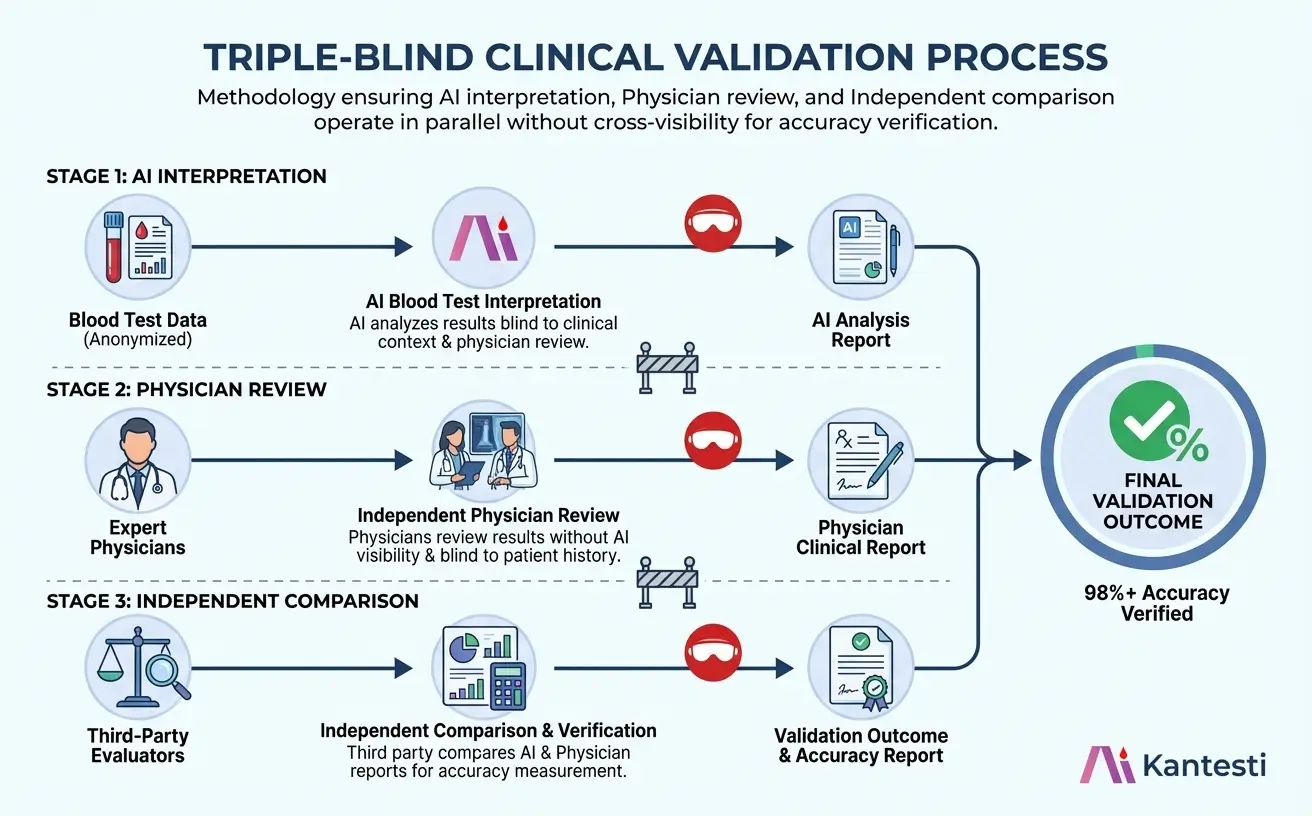
Trippelblind valideringsmetodik: AI-tolkning (steg 1), läkargranskning (steg 2) och oberoende jämförelse (steg 3) fungerar parallellt utan korsvisibilitet.
Validerad prestanda per testkategori
Prestandamätvärden validerade genom trippelblind klinisk granskning av över 1 000 000 testfall. Resultaten visar konsekvent noggrannhet i alla större biomarkörkategorier.
Övergripande noggrannhetssammanfattning
Aggregerad noggrannhet: 98,7% — Viktat medelvärde för alla testkategorier baserat på trippelblind läkarkonkordans. Prestandan för enskilda kategorier varierar från 98,1% till 99,3%-känslighet. Se rapport §4.1, tabell 2
Korrelation mellan kliniskt utfall: 87% — Longitudinell korrelation med bekräftade diagnoser i uppföljningsstudier i verkligheten. Se rapport §4.3
| Testkategori | Känslighet | Specificitet | Provstorlek |
|---|---|---|---|
| Fullständigt blodvärde (CBC) | 99.3% | 99.0% | 285,000 |
| Omfattande metabolisk panel | 99.1% | 98.9% | 198,000 |
| Lipidpanel | 98.8% | 98.5% | 167,000 |
| Sköldkörtelfunktion | 98.4% | 98.1% | 142,000 |
| Leverfunktionstester | 98.9% | 98.6% | 124,000 |
| Njurfunktionspanelen | 99.2% | 99.0% | 84,000 |
Befolkningskonsistens
Valideringsresultaten visar att 99%-noggrannheten är konsekvent över alla demografiska grupper oavsett etnicitet, ålder, kön eller geografisk region. Populationsproportionellt urval säkerställer representativ täckning i 197 länder.
Global valideringsdatauppsättningsdistribution
Våra träningsdataset med 15 miljoner exempel och fler än 1 miljon valideringsfall är distribuerade över alla större globala regioner för att säkerställa en noggrannhet som är representativ för befolkningen.
Medicinsk rådgivande nämnd
Vår medicinska rådgivande nämnd tillhandahåller klinisk tillsyn över all utveckling och validering av AI-algoritmer. Styrelseledamöterna representerar olika specialiteter från flera länder och har tillsammans över 180 års expertis inom klinisk medicin.
Thomas Klein, läkare
Chefsläkare (CMO) Klinisk hematologi och AI-diagnostikDr. Sarah Mitchell, läkare, PhD
Chefsmedicinsk rådgivare Klinisk patologi och laboratoriemedicinProfessor Dr. Hans Weber
Senior medicinsk rådgivare Laboratoriemedicin och klinisk kemiDr. Maria Rodriguez, läkare, MPH
Medicinsk rådgivare Internmedicin och förebyggande medicinDr. Chen Wei, läkare, magisterexamen
Medicinsk rådgivare Endokrinologi och metabol medicinTräffa hela vår medicinska rådgivande nämnd med detaljerade profiler, meriter och forskningsbakgrund.
Visa alla rådgivare →Kontinuerlig kvalitetsövervakning
Validering efter driftsättning fortsätter genom strukturerade övervakningsprotokoll. Prestanda i verkligheten mäts mot kliniska resultat, med återkopplingsslingor som möjliggör kontinuerlig förbättring.
Månatliga resultatrapporter
Omfattande noggrannhetsanalys över alla biomarkörkategorier, demografiska segment och geografiska regioner. Trendidentifiering möjliggör proaktiv kvalitetshantering.
Interlaboratorieöverensstämmelse
Testning av över 500 laboratoriesystem validerar konsekvent prestanda oavsett utrustningstillverkare, metod eller kalibreringsstandarder.
Kliniska utfallsstudier
Longitudinella korrelationsstudier spårar AI-tolkningar mot bekräftade diagnoser och uppnår 87%-korrelation med kliniska utfall över olika patientpopulationer.
Feedback från vårdgivare
Strukturerad integrering av feedback från läkare och laboratoriepersonal. Flaggade tolkningar granskas av den medicinska rådgivande nämnden med korrigeringar integrerade i utbildningen.
Utbildningsdata och kvalitetssäkring
Vår AI-modell är tränad på en av de största kurerade blodprovsdataseten i branschen, med rigorösa kvalitetskontroller som säkerställer dataintegritet och klinisk relevans.
Datasetets sammansättning
- Totalt antal prover15 miljoner
- Geografisk täckning197 länder
- Laboratoriekällor500+ certifierade laboratorier
- Datumintervall2015-2025
- Biomarkörtyper450+ parametrar
Kvalitetskontroller
Flerstegs datakvalitetssäkring:
- Endast ISO 15189-certifierade laboratoriekällor
- Borttagning av ofullständiga eller skadade register
- Avvikande detektion av preanalytiska fel
- Proveniensverifiering för alla datamängder
- HIPAA/GDPR-kompatibel anonymisering
Teknik- och efterlevnadspartners
Vår valideringsinfrastruktur och AI-utveckling stöds genom partnerskap med branschledande teknikleverantörer.
Microsoft FoundersHub
Molninfrastruktur och AI-utvecklingsplattform i företagsklass som stöder skalbara valideringsarbetsflöden.
NVIDIA Inception Program
GPU-beräkningsresurser och AI-modelloptimering möjliggör effektiv träning på fler än 15 miljoner exempeldatamängder.
Google Cloud AI
Maskininlärningsinfrastruktur som stöder distribuerad modellträning och realtidsinferens.
Cloudflare
Globalt edge-nätverk som garanterar säker åtkomst med låg latens i 197 länder.
SOC 2 Typ II-kontroller
Säkerhetskontroller i linje med AICPA-standarder
ISO 27001-anpassad
Kontroller för informationssäkerhetshantering
HIPAA-anpassade kontroller
Skyddsåtgärder för dataskydd inom hälso- och sjukvården i USA
GDPR-kompatibel
Europeiska dataskyddsförordningen
Lämplig användning och begränsningar
Transparens kring möjligheter och begränsningar är avgörande för ansvarsfull AI-användning inom hälso- och sjukvården. Kantesti är utformat som ett beslutsstödsverktyg för att komplettera – inte ersätta – professionell medicinsk bedömning.
Informationen är inte åtkommen
Vår AI tolkar biomarkördata isolerat. Följande kliniska kontext är inte tillgänglig för systemet:
- Komplett patienthistoria
- Nuvarande läkemedel och potentiella interaktioner
- Fysisk undersökningsresultat
- Genetiska faktorer och familjehistoria
- Livsstilsfaktorer (såvida inte användaren tillhandahåller dem)
Variationer i laboratoriemetodik
Referensområdena varierar mellan laboratorier på grund av skillnader i utrustning och kalibreringsstandarder. Vår databas med över 45 000 laboratoriespecifika intervall täcker de flesta variationer, men användare bör kontrollera att de extraherade värdena matchar deras ursprungliga rapport.
Överväganden gällande dokumentkvalitet
OCR-noggrannheten beror på dokumentkvaliteten. Handskrivna resultat eller skanningar med låg upplösning kan påverka värdeutvinningen. Manuell korrigering är tillgänglig för alla extraherade värden före analys.
Medicinsk ansvarsfriskrivning
Kantesti är ett AI-baserat informationsverktyg som tolkar blodprovsresultat baserat på etablerade medicinska referensintervall och kliniska riktlinjer. Det är INTE en medicinteknisk produkt och varken diagnostiserar, behandlar, botar eller förebygger någon sjukdom.
Informationen som tillhandahålls är endast avsedd för utbildnings- och informationsändamål och bör inte betraktas som medicinsk rådgivning. Rådfråga alltid kvalificerad sjukvårdspersonal innan du fattar beslut om din hälsa eller behandling.
Vid medicinska nödsituationer, kontakta omedelbart räddningstjänsten. Kantesti är inte avsedd för nödsituationer.
Intressekonflikter och finansieringsupplysningar
Denna valideringsdokumentation publiceras av Kantesti/PIYA AI. Medlemmar i den medicinska rådgivande nämnden får ersättning för sina rådgivande roller. Marknadschef (Thomas Klein, MD) är heltidsanställd hos Kantesti AI. All valideringsdata har verifierats oberoende genom trippelblind metodik. Ingen extern finansiering har erhållits för valideringsstudier. Företaget är självfinansierat genom intäkts- och teknikpartnerskap med Microsoft, NVIDIA, Google Cloud och Cloudflare.
Vanliga frågor om medicinsk validering
Vad betyder "trippelblind validering"?
Trippelblind validering innebär att tre oberoende parter analyserar samma data utan att känna till varandras slutsatser. Vår AI tolkar blodprover utan klinisk kontext, läkare granskar oberoende av varandra utan att se AI-resultaten, och ett tredje team jämför resultaten utan att veta vilka som kom från AI respektive läkare. Detta eliminerar bekräftelsebias och säkerställer objektiv noggrannhet i mätningarna.
Hur ofta uppdateras AI-modellen?
Vår modell genomgår kvartalsvis omskolning med nya validerade data, uppdaterade kliniska riktlinjer och ny biomarkörforskning. Varje uppdatering klarar hela trippelblinda valideringsprotokollet innan driftsättning. Uppdateringar som inte uppfyller vår noggrannhetströskel avvisas.
Varför varierar noggrannheten mellan testkategorier?
Vissa biomarkörer har mer standardiserade referensintervall globalt (som elektrolyter), medan andra varierar mer mellan laboratorier och populationer (som sköldkörtelhormoner). Kategorier med mer variation visar något lägre noggrannhet på grund av den inneboende komplexiteten i tolkningen.
Kan jag lita på AI-tolkning för medicinska beslut?
Kantesti är utformat som ett beslutsstödsverktyg, inte en ersättning för professionell medicinsk bedömning. Vår AI ger validerade tolkningar baserade på etablerade referensintervall, men klinisk kontext – inklusive din sjukdomshistoria, mediciner och symtom – kräver läkarutvärdering för behandlingsbeslut. Rådgör alltid med din vårdgivare.
Hur hanteras populationsdiversitet i validering?
Våra träningsdata omfattar 15 miljoner stickprov proportionellt fördelade över 197 länder, med populationsviktat urval som säkerställer representation från alla större etniska och geografiska grupper. Kvartalsvisa rättviserevisioner verifierar noggrannhet och konsekvens mellan demografiska grupper, med 99%-konsekvens upprätthållen över alla befolkningssegment.
Vad händer om AI:n gör ett fel?
Vårdgivare och användare kan flagga tolkningar för granskning av den medicinska rådgivande nämnden. Flaggade fall analyseras av vår marknadschef Thomas Klein, MD, och det medicinska teamet. Om fel bekräftas integreras korrigeringar i framtida utbildningscykler. Vår kontinuerliga övervakning spårar verkliga resultat för att identifiera och åtgärda systematiska problem proaktivt.
Var kan jag hitta den fullständiga valideringsrapporten?
Vår fullständiga valideringsmetodik finns dokumenterad i den tekniska rapporten "Clinical Validation Framework for AI-Powered Blood Test Interpretation" (rapport-ID: KANTESTI-TR-2025-001, DOI: 10.5281/kantesti.2025.mv2). Den fullständiga rapporten finns tillgänglig via DOI-länken, på ResearchGate och som en nedladdningsbar PDF från vår webbplats.
Vem granskar det medicinska innehållet på Kantesti?
Allt medicinskt innehåll är skrivet och granskat av Thomas Klein, MD, vår chefsläkare. Dr. Klein är en legitimerad klinisk hematolog knuten till Istanbul Nisantasi universitets hematologiska institution, med över 15 års erfarenhet av laboratoriemedicin och AI-assisterad diagnostik. Ytterligare tillsyn tillhandahålls av vår medicinska rådgivande nämnd med 12 medlemmar.
Erfarenhetsvaliderad AI-blodprovsanalys
Gå med miljontals användare världen över som litar på Kantestis AI-blodtestanalysator för kliniskt validerad tolkning av blodprover på över 75 språk.
Företagens transparens
Vi tror på fullständig transparens kring vilka vi är och hur vi arbetar. Nedan hittar du information om våra företagsregistreringar och information om ledarskapet.
Kantesti AI - PIYA AI
Juridisk enhet: PIYA AI (Kantesti Brand Owner)
Företagstyp: AI-hälsovårdsteknik
Grundad: 2019
Huvudkontor: Köln, Tyskland
Kontakta: [email protected]
Telefon: +49 177 497 4039
Ledarskap
Grundare och VD: Julian Emirhan Bulut
Visionär entreprenör som leder AI-innovation inom hälso- och sjukvårdsteknik. Bygger tillgängliga verktyg för tolkning av blodprover för global hälsoförbättring.
Anslut på LinkedInÖverläkare: Thomas Klein, läkare
Styrelsecertifierad klinisk hematolog som leder medicinsk validering och klinisk tillsyn.
Efterlevnad och certifieringar
Dataskydd: GDPR-kompatibel (EU)
Hälso- och sjukvårdens integritet: HIPAA-anpassade skyddsåtgärder (USA)
Säkerhet: SOC 2 Typ II-kontroller
Kvalitetsledning: ISO 27001-anpassad
Medicinteknisk anordning: Inte klassificerad som medicinteknisk produkt - Endast informationsverktyg
Referenser och standarder
Vår valideringsmetodik och kliniska standarder är baserade på etablerade medicinska riktlinjer och internationella standarder.
- [1] Världshälsoorganisationen (WHO). Användning av glykerat hemoglobin (HbA1c) vid diagnos av diabetes mellitus. Genève: WHO; 2011. Tillgänglig från: https://www.who.int/diabetes/publications/diagnosis_diabetes2011/en/
- [2] Internationella standardiseringsorganisationen. ISO 15189:2022 Medicinska laboratorier — Krav på kvalitet och kompetens. Genève: ISO; 2022. https://www.iso.org/standard/76677.html
- [3] Institutet för kliniska och laboratoriestandarder (CLSI). EP09c: Jämförelse av mätprocedurer och biasuppskattning med hjälp av patientprover. 3:e uppl. Wayne, PA: CLSI; 2018.
- [4] Nationella hälsoinstituten (NIH). Referensområden för blodprover. Bethesda, MD: NIH; Uppdaterad 2024. Tillgänglig från: MedlinePlus
- [5] Amerikanska föreningen för klinisk kemi (AACC). Referensområden för laboratorietester. Washington, DC: AACC; 2024. https://www.aacc.org/
- [6] Internationella federationen för klinisk kemi (IFCC). Referensmätningsprocedurer. Milano: IFCC; 2023. https://www.ifcc.org/
- [7] Klein T. Kliniskt valideringsramverk för AI-driven blodprovstolkning: Trippelblind valideringsmetodik, prestandamått och kvalitetssäkringsprotokoll. Teknisk rapport KANTESTI-TR-2025-001, version 2.0. Kantesti AI; 2025. DOI: 10.5281/kantesti.2025.mv2
- [8] Amerikanska hälso- och socialdepartementet. HIPAA-sekretessregel. 45 CFR del 160 och underavsnitt A och E i del 164. Washington, DC: HHS; 2013.
- [9] Europaparlamentet och rådet. Allmänna dataskyddsförordningen (GDPR). Förordning (EU) 2016/679. Bryssel: EU; 2016.