Medische validatie en klinische normen voor AI-bloedtestanalyse
Driedubbelblinde klinische validatiemethodologie, toezicht door gecertificeerde artsen en praktijkgerichte correlatiestudies voor uitkomsten die de meest vertrouwde bron vormen voor 's werelds meest betrouwbare AI-bloedtestanalysator.
Primair bewijsmateriaal en documentatie
De beweringen en validatiegegevens op deze pagina zijn gedocumenteerd in ons technisch rapport (onderworpen aan collegiale toetsing). De volledige methodologie en het bewijsmateriaal vindt u hieronder.
Klinisch validatiekader voor AI-gestuurde interpretatie van bloedtesten
Methodologie voor drievoudige blinde validatie, prestatiemaatstaven en kwaliteitsborgingsprotocollen
Klinisch validatiekader
Kantesti's AI-bloedtestinterpretatie Het platform ondergaat strenge medische validatie om klinische betrouwbaarheid te garanderen. Ons meerlagige validatieproces combineert machine learning-validatie met traditionele klinische beoordelingsmethodologieën.
Elke algoritme-update ondergaat een drievoudig blinde klinische validatie voordat het in productie gaat. Deze pagina documenteert ons volledige validatiekader, de structuur voor medisch toezicht en de protocollen voor continue kwaliteitsbewaking.
Drievoudig blind klinisch validatieproces
Onze validatiemethodologie elimineert bevestigingsbias door middel van een onafhankelijk beoordelingsproces in drie fasen. Elke fase werkt zonder kennis van de conclusies van de andere fasen, wat een objectieve nauwkeurigheid van de meting garandeert.
AI-interpretatie
Het AI-systeem analyseert bloedtestresultaten zonder toegang tot klinische diagnose, patiëntgeschiedenis of aantekeningen van de arts. Deze blinde analyse zorgt ervoor dat de interpretatie van de AI uitsluitend gebaseerd is op biomarkergegevens en vastgestelde referentiewaarden.
- Geen toegang tot klinische diagnose
- Bevolkingsgecorrigeerde referentiebereiken
- Multi-parameter correlatieanalyse
Beoordeling door artsen
Gecertificeerde pathologen beoordelen onafhankelijk dezelfde bloedtestresultaten. Artsen hebben geen toegang tot AI-interpretaties, waardoor hun klinische oordeel onbevooroordeeld blijft.
- Gecertificeerde klinische pathologen
- Geen zicht op de AI-output
- Gestandaardiseerde beoordelingsprotocollen
Onafhankelijke vergelijking
Een extern klinisch team vergelijkt de AI-output met de consensus van artsen, zonder te weten welke interpretatie uit welke bron komt. Afwijkingen leiden tot extra beoordelingscycli.
- Methodologie voor blinde vergelijking
- Statistische concordantieanalyse
- Volledige audit trail-documentatie
Workflow voor driedubbelblinde validatie
Ons validatieproces garandeert een objectieve nauwkeurigheidsbeoordeling via onafhankelijke, parallelle beoordelingsstromen die pas bij de uiteindelijke vergelijking samenkomen.
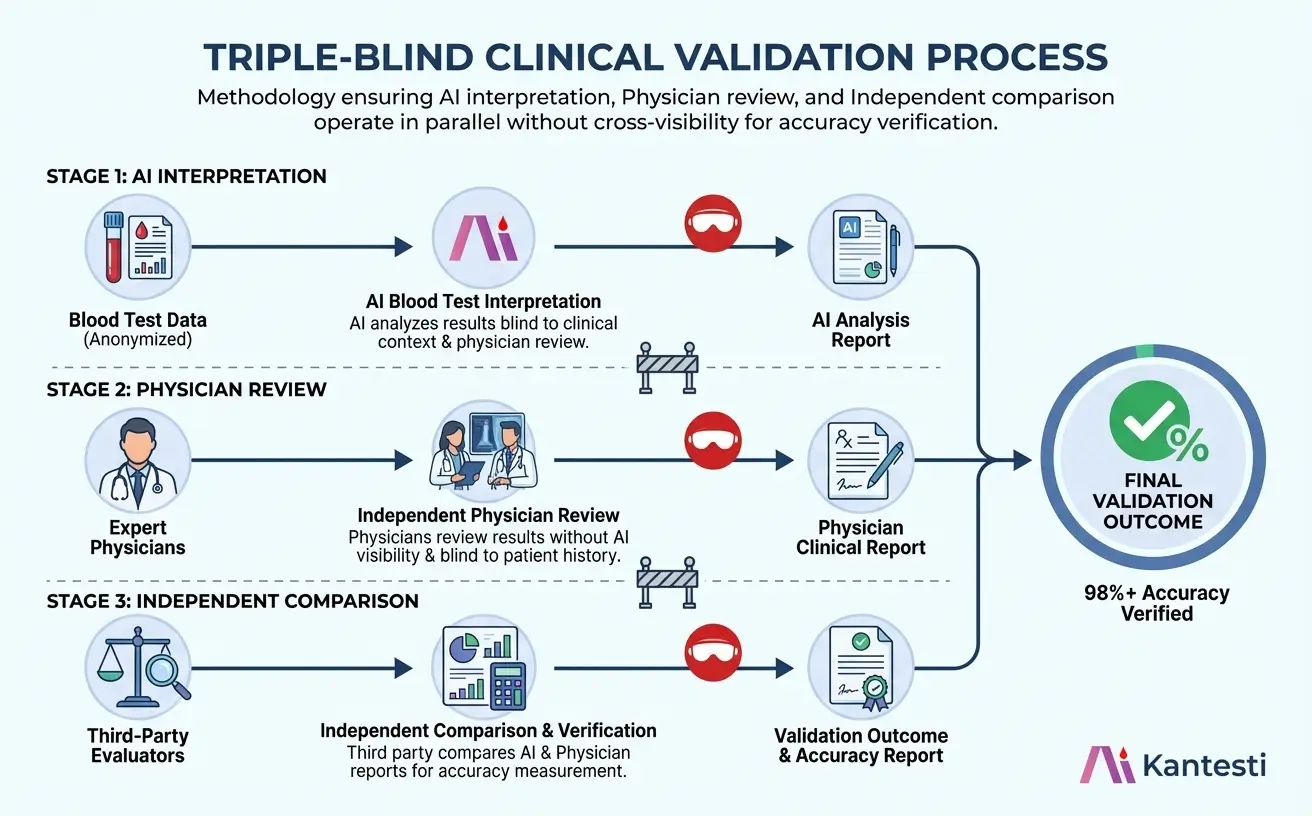
Triple-blind validatiemethodologie: AI-interpretatie (fase 1), beoordeling door de arts (fase 2) en onafhankelijke vergelijking (fase 3) vinden parallel plaats zonder dat er sprake is van wederzijdse zichtbaarheid.
Gevalideerde prestaties per testcategorie
Prestatiegegevens gevalideerd door middel van triple-blinde klinische beoordeling van meer dan 1.000.000 testcases. De resultaten tonen consistente nauwkeurigheid in alle belangrijke biomarkercategorieën.
Samenvatting van de algehele nauwkeurigheid
Geaggregeerde nauwkeurigheid: 98,7% — Gewogen gemiddelde over alle testcategorieën op basis van triple-blinde overeenstemming tussen artsen. De prestaties per categorie variëren van 98,1% tot 99,3% gevoeligheid. Zie Rapport §4.1, Tabel 2
Klinische uitkomstcorrelatie: 87% — Longitudinale correlatie met bevestigde diagnoses in real-world follow-up studies. Zie Rapport §4.3
| Testcategorie | Gevoeligheid | Specificiteit | Steekproefgrootte |
|---|---|---|---|
| Volledig bloedbeeld (CBC) | 99.3% | 99.0% | 285,000 |
| Uitgebreid metabolisch paneel | 99.1% | 98.9% | 198,000 |
| Lipidenpaneel | 98.8% | 98.5% | 167,000 |
| Schildklierfunctie | 98.4% | 98.1% | 142,000 |
| Leverfunctietesten | 98.9% | 98.6% | 124,000 |
| Nierfunctiepaneel | 99.2% | 99.0% | 84,000 |
Bevolkingsconsistentie
Validatieresultaten tonen consistente 99%-nauwkeurigheid aan in alle demografische groepen, ongeacht etniciteit, leeftijd, geslacht of geografische regio. Populatieproportionele steekproeven zorgen voor een representatieve dekking in 197 landen.
Wereldwijde distributie van validatiegegevenssets
Onze trainingsdataset van 15 miljoen voorbeelden en meer dan 1 miljoen validatiegevallen zijn verspreid over alle belangrijke wereldregio's om een representatieve nauwkeurigheid voor de bevolking te garanderen.
Medische Adviesraad
Onze medische adviesraad houdt klinisch toezicht op de ontwikkeling en validatie van alle AI-algoritmen. De leden van de raad vertegenwoordigen diverse specialismen uit meerdere landen en beschikken samen over meer dan 180 jaar expertise in de klinische geneeskunde.
Thomas Klein, arts
Hoofdmedisch adviseur (CMO) Klinische hematologie en AI-diagnostiekDr. Sarah Mitchell, MD, PhD
Hoofd medisch adviseur Klinische Pathologie & LaboratoriumgeneeskundeProf. dr. Hans Weber
Senior medisch adviseur Laboratoriumgeneeskunde en klinische chemieDr. Maria Rodriguez, MD, MPH
Medisch adviseur Interne geneeskunde en preventieve geneeskundeDr. Chen Wei, MD, MSc
Medisch adviseur Endocrinologie en metabole geneeskundeMaak kennis met onze volledige medische adviesraad met gedetailleerde profielen, referenties en onderzoeksachtergronden.
Bekijk alle adviseurs →Continue kwaliteitsbewaking
Validatie na implementatie wordt voortgezet via gestructureerde monitoringprotocollen. De prestaties in de praktijk worden vergeleken met klinische resultaten, met feedbacklussen die continue verbetering mogelijk maken.
Maandelijkse prestatieverslagen
Uitgebreide nauwkeurigheidsanalyse in alle biomarkercategorieën, demografische segmenten en geografische regio's. Trendidentificatie maakt proactief kwaliteitsmanagement mogelijk.
Interlaboratoriumconcordantie
Door tests uit te voeren op meer dan 500 laboratoriumsystemen wordt gegarandeerd dat de prestaties consistent zijn, ongeacht de fabrikant van de apparatuur, de methodologie of de kalibratienormen.
Klinische uitkomststudies
Longitudinale correlatieonderzoeken vergelijken AI-interpretaties met bevestigde diagnoses en bereiken een 87%-correlatie met klinische uitkomsten in diverse patiëntenpopulaties.
Feedback van zorgverleners
Gestructureerde feedbackintegratie van artsen en laboratoriumprofessionals. Gemarkeerde interpretaties worden beoordeeld door de Medische Adviesraad en correcties worden geïntegreerd in de training.
Trainingsgegevens en kwaliteitsborging
Ons AI-model is getraind op een van de grootste samengestelde datasets met bloedtestgegevens in de branche, met strenge kwaliteitscontroles die de integriteit en klinische relevantie van de gegevens waarborgen.
Samenstelling van de dataset
- Totaal aantal monsters15 miljoen
- Geografische dekking197 landen
- LaboratoriumbronnenMeer dan 500 gecertificeerde laboratoria
- Datumbereik2015-2025
- BiomarkertypenMeer dan 450 parameters
Kwaliteitscontroles
Meerfase datakwaliteitsborging:
- Uitsluitend ISO 15189-gecertificeerde laboratoriumbronnen
- Verwijdering van onvolledige of beschadigde gegevens
- Detectie van uitschieters bij pre-analytische fouten
- Herkomstverificatie voor alle datasets
- HIPAA/GDPR-conforme anonimisering
Technologie- en compliancepartners
Onze validatie-infrastructuur en AI-ontwikkeling worden ondersteund door partnerschappen met toonaangevende technologieleveranciers in de sector.
Microsoft FoundersHub
Cloudinfrastructuur en AI-ontwikkelingsplatform op ondernemingsniveau ter ondersteuning van schaalbare validatieworkflows.
NVIDIA Inception-programma
GPU-rekenkracht en AI-modeloptimalisatie maken efficiënte training mogelijk met meer dan 15 miljoen voorbeelddatasets.
Google Cloud AI
Machine learning-infrastructuur die gedistribueerde modeltraining en realtime-inferentie ondersteunt.
Cloudflare
Wereldwijd edge-netwerk dat veilige toegang met lage latentie garandeert in 197 landen.
SOC 2 Type II-controles
Beveiligingsmaatregelen in overeenstemming met AICPA-normen.
ISO 27001-conform
Informatiebeveiligingsbeheercontroles
HIPAA-conforme controles
Amerikaanse waarborgen voor de bescherming van gezondheidsgegevens
AVG-conform
Europese verordening gegevensbescherming
Correct gebruik en beperkingen
Transparantie over mogelijkheden en beperkingen is essentieel voor verantwoorde inzet van AI in de gezondheidszorg. Kantesti is bedoeld als hulpmiddel ter ondersteuning van besluitvorming, ter aanvulling op, en niet ter vervanging van, professioneel medisch oordeel.
Informatie niet toegankelijk
Onze AI interpreteert biomarkergegevens geïsoleerd. De volgende klinische context is niet beschikbaar voor het systeem:
- Volledige medische geschiedenis van de patiënt
- Huidige medicijnen en mogelijke interacties
- Bevindingen bij lichamelijk onderzoek
- Genetische factoren en familiegeschiedenis
- Leefstijlfactoren (tenzij door de gebruiker verstrekt)
Variaties in laboratoriummethodologie
Referentiebereiken variëren per laboratorium vanwege verschillen in apparatuur en kalibratienormen. Onze database met meer dan 45.000 laboratoriumspecifieke bereiken dekt de meeste variaties, maar gebruikers dienen te controleren of de geëxtraheerde waarden overeenkomen met hun oorspronkelijke rapport.
Overwegingen met betrekking tot documentkwaliteit
De nauwkeurigheid van OCR is afhankelijk van de documentkwaliteit. Handgeschreven resultaten of scans met een lage resolutie kunnen de waarde-extractie beïnvloeden. Handmatige correctie is beschikbaar voor alle geëxtraheerde waarden vóór de analyse.
Medische disclaimer
Kantesti is een AI-gestuurde informatietool die bloedtestresultaten interpreteert op basis van vastgestelde medische referentiewaarden en klinische richtlijnen. Het is GEEN medisch hulpmiddel en diagnosticeert, behandelt, geneest of voorkomt geen ziekten.
De verstrekte informatie is uitsluitend bedoeld voor educatieve en informatieve doeleinden en mag niet worden beschouwd als medisch advies. Raadpleeg altijd een gekwalificeerde zorgverlener voordat u beslissingen neemt over uw gezondheid of behandeling.
Neem bij medische noodgevallen onmiddellijk contact op met de hulpdiensten. Kantesti is niet ontworpen voor noodsituaties.
Openbaarmaking van belangenconflicten en financiering
Deze validatiedocumentatie is gepubliceerd door Kantesti/PIYA AI. Leden van de medische adviesraad ontvangen een vergoeding voor hun adviserende rol. De CMO (Thomas Klein, MD) is een fulltime medewerker van Kantesti AI. Alle validatiegegevens zijn onafhankelijk geverifieerd met behulp van een drievoudig blinde methodologie. Er is geen externe financiering ontvangen voor de validatiestudies. Het bedrijf wordt zelf gefinancierd door middel van inkomsten en technologische partnerschappen met Microsoft, NVIDIA, Google Cloud en Cloudflare.
Veelgestelde vragen over medische validatie
Wat betekent "triple-blind validatie"?
Drievoudig blinde validatie betekent dat drie onafhankelijke partijen dezelfde gegevens analyseren zonder elkaars conclusies te kennen. Onze AI interpreteert bloedtesten zonder klinische context, artsen beoordelen de resultaten onafhankelijk van elkaar zonder de output van de AI te zien, en een derde team vergelijkt de resultaten zonder te weten welke afkomstig zijn van de AI en welke van de artsen. Dit elimineert bevestigingsbias en garandeert een objectieve meting van de nauwkeurigheid.
Hoe vaak wordt het AI-model bijgewerkt?
Ons model wordt elk kwartaal bijgeschoold met nieuwe gevalideerde gegevens, bijgewerkte klinische richtlijnen en nieuw onderzoek naar biomarkers. Elke update doorloopt het volledige triple-blind validatieprotocol voordat deze wordt geïmplementeerd. Updates die niet aan onze nauwkeurigheidsdrempel voldoen, worden afgewezen.
Waarom varieert de nauwkeurigheid per testcategorie?
Sommige biomarkers hebben wereldwijd meer gestandaardiseerde referentiewaarden (zoals elektrolyten), terwijl andere meer variëren tussen laboratoria en populaties (zoals schildklierhormonen). Categorieën met meer variatie vertonen een iets lagere nauwkeurigheid vanwege de inherente complexiteit van de interpretatie.
Kan ik vertrouwen op AI-interpretatie voor medische beslissingen?
Kantesti is ontworpen als hulpmiddel voor besluitvorming, niet als vervanging voor professioneel medisch oordeel. Onze AI levert gevalideerde interpretaties op basis van vastgestelde referentiewaarden, maar de klinische context – inclusief uw medische geschiedenis, medicatie en symptomen – vereist een beoordeling door een arts voor behandelbeslissingen. Raadpleeg altijd uw zorgverlener.
Hoe wordt er bij de validatie rekening gehouden met populatiediversiteit?
Onze trainingsdataset omvat 15 miljoen samples, proportioneel verdeeld over 197 landen. De steekproefmethode is gewogen naar bevolkingsomvang, waardoor representatie van alle belangrijke etnische en geografische groepen is gewaarborgd. Kwartaallijkse controles verifiëren de consistentie van de nauwkeurigheid over de verschillende demografische groepen, waarbij de 99%-consistentie wordt gehandhaafd voor alle bevolkingssegmenten.
Wat gebeurt er als de AI een fout maakt?
Zorgverleners en gebruikers kunnen interpretaties markeren voor beoordeling door de Medische Adviesraad. Gemarkeerde gevallen worden geanalyseerd door onze Chief Medical Officer, Dr. Thomas Klein, en het medisch team. Als fouten worden bevestigd, worden correcties opgenomen in toekomstige trainingscycli. Onze continue monitoring volgt de prestaties in de praktijk om systematische problemen proactief te identificeren en aan te pakken.
Waar kan ik het volledige validatierapport vinden?
Onze volledige validatiemethodologie is gedocumenteerd in het technische rapport "Clinical Validation Framework for AI-Powered Blood Test Interpretation" (Rapport-ID: KANTESTI-TR-2025-001, DOI: 10.5281/kantesti.2025.mv2). Het volledige rapport is beschikbaar via de DOI-link, op ResearchGate en als downloadbaar PDF-bestand op onze website.
Wie beoordeelt de medische inhoud op Kantesti?
Alle medische inhoud wordt geschreven en beoordeeld door Thomas Klein, MD, onze Chief Medical Officer. Dr. Klein is een gecertificeerd klinisch hematoloog verbonden aan de afdeling Hematologie van de Istanbul Nisantasi Universiteit, met meer dan 15 jaar ervaring in laboratoriumgeneeskunde en AI-ondersteunde diagnostiek. Aanvullend toezicht wordt geboden door onze 12-koppige medische adviesraad.
Ervaar gevalideerde AI-bloedtestanalyse
Sluit u aan bij miljoenen gebruikers wereldwijd die u vertrouwen Kantesti's AI-bloedtestanalysator voor klinisch gevalideerde bloedtestinterpretatie in meer dan 75 talen.
Transparantie van bedrijven
Wij geloven in volledige transparantie over wie we zijn en hoe we werken. Hieronder vindt u onze bedrijfsregistratiegegevens en informatie over ons leiderschap.
Kantesti AI - PIYA AI
Juridische entiteit: PIYA AI (Kantesti-merkeigenaar)
Bedrijfstype: AI-gezondheidszorgtechnologie
Opgericht: 2019
Hoofdkwartier: Keulen, Duitsland
Contact: [email protected]
Telefoon: +49 177 497 4039
Leiderschap
Oprichter en CEO: Julian Emirhan Bulut
Visionair ondernemer die AI-innovatie in de gezondheidszorg leidt. Ontwikkelt toegankelijke tools voor de interpretatie van bloedtesten ter verbetering van de wereldwijde gezondheid.
Maak verbinding op LinkedInHoofdmedisch adviseur: Thomas Klein, arts
Gecertificeerd klinisch hematoloog, verantwoordelijk voor medische validatie en klinisch toezicht.
Naleving en certificeringen
Gegevensbescherming: AVG-conform (EU)
Privacy in de gezondheidszorg: HIPAA-conforme beveiligingsmaatregelen (VS)
Beveiliging: SOC 2 Type II-controles
Kwaliteitsmanagement: ISO 27001-conform
Medisch hulpmiddel: Niet geclassificeerd als medisch hulpmiddel - Alleen informatief hulpmiddel
Referenties en normen
Onze validatiemethodologie en klinische normen zijn gebaseerd op gevestigde medische richtlijnen en internationale standaarden.
- [1] Wereldgezondheidsorganisatie (WHO). Het gebruik van geglyceerd hemoglobine (HbA1c) bij de diagnose van diabetes mellitus. Genève: WHO; 2011. Beschikbaar via: https://www.who.int/diabetes/publications/diagnosis_diabetes2011/en/
- [2] Internationale Organisatie voor Standaardisatie. ISO 15189:2022 Medische laboratoria — Eisen voor kwaliteit en competentie. Genève: ISO; 2022. https://www.iso.org/standard/76677.html
- [3] Clinical and Laboratory Standards Institute (CLSI). EP09c: Vergelijking van meetprocedures en schatting van vertekening met behulp van patiëntenmonsters. 3e druk. Wayne, PA: CLSI; 2018.
- [4] Nationale Instituten voor Volksgezondheid (NIH). Referentiewaarden voor bloedonderzoek. Bethesda, MD: NIH; Bijgewerkt in 2024. Beschikbaar via: MedlinePlus
- [5] Amerikaanse Vereniging voor Klinische Chemie (AACC). Referentiewaarden voor laboratoriumtests. Washington, DC: AACC; 2024. https://www.aacc.org/
- [6] Internationale Federatie voor Klinische Chemie (IFCC). Referentiemeetprocedures. Milaan: IFCC; 2023. https://www.ifcc.org/
- [7] Klein T. Klinisch validatiekader voor AI-gestuurde interpretatie van bloedtesten: drievoudig blinde validatiemethodologie, prestatiemaatstaven en kwaliteitsborgingsprotocollen. Technisch rapport KANTESTI-TR-2025-001, versie 2.0. Kantesti AI; 2025. DOI: 10.5281/kantesti.2025.mv2
- [8] Amerikaans ministerie van Volksgezondheid en Sociale Zaken. HIPAA-privacyregelgeving. 45 CFR Deel 160 en Subdelen A en E van Deel 164. Washington, DC: HHS; 2013.
- [9] Europees Parlement en Raad. Algemene Verordening Gegevensbescherming (AVG). Verordening (EU) 2016/679. Brussel: EU; 2016.