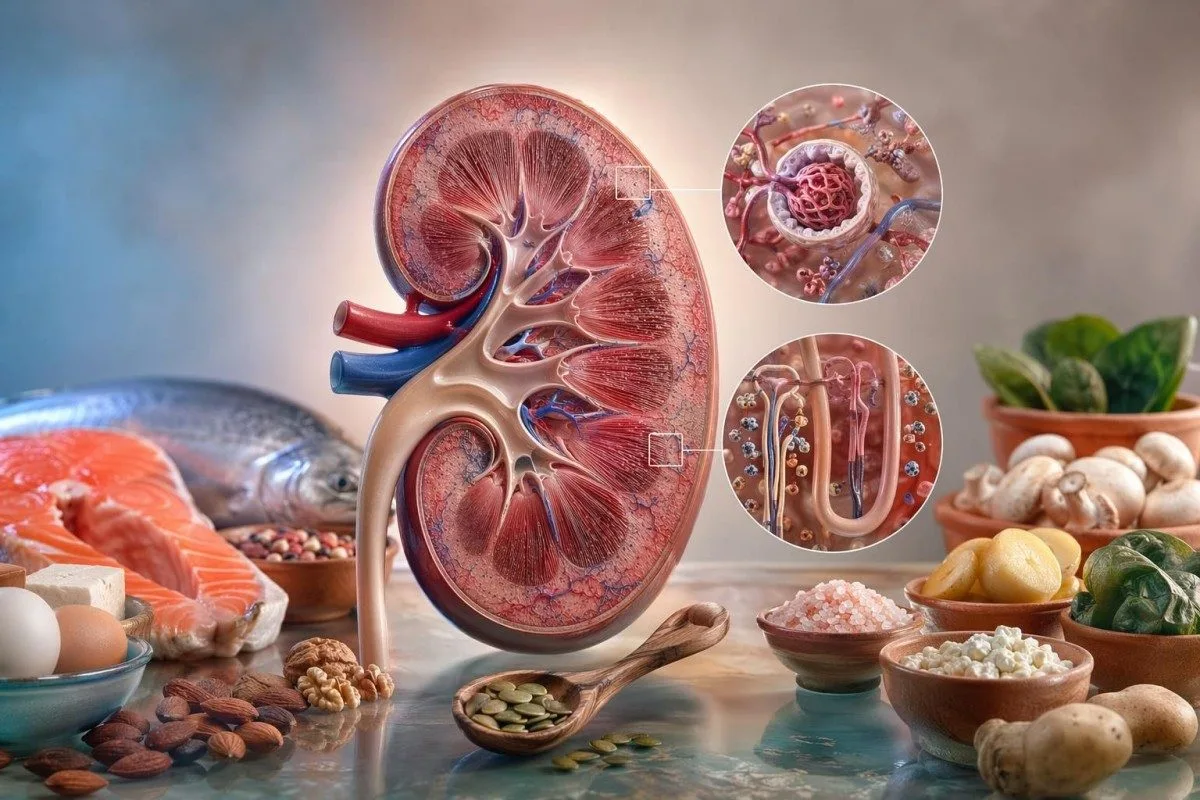
โภชนาการสำหรับไตไม่ใช่ “รายการอาหาร” เดี่ยวๆ ตัวเลือกที่ปลอดภัยที่สุดขึ้นอยู่กับ eGFR, อัลบูมินในปัสสาวะ, โพแทสเซียม, ไบคาร์บอเนต, ฟอสเฟต, ความดันโลหิต, ยาที่ใช้ และผลตรวจเดิมของคุณที่กำลังทำอยู่แล้ว.
คู่มือนี้เขียนภายใต้การนำของ นายแพทย์โทมัส ไคลน์ โดยความร่วมมือกับ คณะกรรมการที่ปรึกษาทางการแพทย์ของ Kantesti AI, รวมถึงบทความจากศาสตราจารย์ ดร. ฮันส์ เวเบอร์ และการตรวจสอบทางการแพทย์โดย ดร. ซาราห์ มิตเชลล์ แพทย์หญิงและด็อกเตอร์.

โทมัส ไคลน์, แพทย์
หัวหน้าเจ้าหน้าที่ทางการแพทย์ บริษัท Kantesti AI
ดร. โธมัส ไคลน์ เป็นแพทย์ผู้เชี่ยวชาญด้านโลหิตวิทยาและอายุรศาสตร์ที่ได้รับการรับรองจากคณะกรรมการ มีประสบการณ์มากกว่า 15 ปีในด้านเวชศาสตร์ห้องปฏิบัติการและการวิเคราะห์ทางคลินิกที่ช่วยด้วย AI ในฐานะ Chief Medical Officer ของ Kantesti AI เขาเป็นผู้นำกระบวนการตรวจสอบความถูกต้องทางคลินิก และดูแลความแม่นยำทางการแพทย์ของเครือข่ายประสาทเทียม 2.78 พารามิเตอร์ของเรา ดร. ไคลน์ได้ตีพิมพ์อย่างกว้างขวางเกี่ยวกับการผลตรวจอ่านไบโอมาร์กเกอร์และการวินิจฉัยทางห้องปฏิบัติการในวารสารการแพทย์ที่ผ่านการตรวจสอบโดยผู้ทรงคุณวุฒิ.

ซาราห์ มิทเชล, แพทย์, ปริญญาเอก
หัวหน้าฝ่ายที่ปรึกษาทางการแพทย์ - พยาธิวิทยาคลินิกและอายุรศาสตร์
ดร. ซาราห์ มิตเชลล์ เป็นแพทย์ผู้เชี่ยวชาญด้านพยาธิวิทยาคลินิกที่ได้รับการรับรองจากคณะกรรมการ มีประสบการณ์มากกว่า 18 ปีในด้านเวชศาสตร์ห้องปฏิบัติการและการวิเคราะห์การวินิจฉัย เธอมีวุฒิบัตรเฉพาะทางด้านเคมีคลินิก และได้ตีพิมพ์อย่างกว้างขวางเกี่ยวกับชุดตรวจไบโอมาร์กเกอร์และการวิเคราะห์ในทางปฏิบัติทางคลินิก.

ศาสตราจารย์ ดร. ฮันส์ เวเบอร์, ปริญญาเอก
ศาสตราจารย์ด้านเวชศาสตร์ห้องปฏิบัติการและชีวเคมีคลินิก
ศ.ดร. ฮันส์ เวเบอร์ มีความเชี่ยวชาญมากกว่า 30 ปีด้านชีวเคมีคลินิก เวชศาสตร์ห้องปฏิบัติการ และงานวิจัยไบโอมาร์กเกอร์ อดีตประธานของสมาคมเคมีคลินิกแห่งเยอรมนี เขาเชี่ยวชาญด้านการวิเคราะห์ชุดตรวจเพื่อการวินิจฉัย การมาตรฐานของไบโอมาร์กเกอร์ และเวชศาสตร์ห้องปฏิบัติการที่ช่วยด้วย AI.
- อัตราการกรองไต (eGFR) ต่ำกว่า 60 mL/min/1.73 m² ติดต่อกันเกิน 3 เดือนบ่งชี้โรคไตเรื้อรัง โดยเฉพาะเมื่อค่า ACR ในปัสสาวะอยู่ที่ 30 mg/g หรือสูงกว่า.
- บัน มักอยู่ที่ 7–20 mg/dL ในผู้ใหญ่; ค่าที่สูงขึ้นหลังการกินโปรตีนสูงอาจเกิดขึ้นได้โดยไม่ทำให้ครีเอตินีนสูงขึ้นตาม.
- ครีเอตินิน อาจเพิ่มขึ้นหลังการกินเนื้อสัตว์ที่ปรุงสุก การเสริมครีเอทีน ภาวะขาดน้ำ การฝึกหนัก หรือไตรเมโทพริม ดังนั้นแนวโน้มจึงสำคัญกว่าค่าเพียงค่าเดียว.
- โซเดียม โดยทั่วไปมักแนะนำให้อยู่ต่ำกว่า 2,000 mg/วันสำหรับ CKD ที่มีความดันโลหิตสูง แต่สำหรับนักกีฬา ผู้ป่วยที่กินโซเดียมต่ำ และผู้สูงอายุบางกลุ่มควรระวังเป็นพิเศษ.
- โพแทสเซียม โดยปกติจะวัดได้ประมาณ 3.5–5.0 mmol/L; อาหารที่มีโพแทสเซียมสูงไม่ได้ถูกห้ามโดยอัตโนมัติ เว้นแต่ผลตรวจ ยา หรือ eGFR ทำให้มีโอกาสเกิดการคั่งค้าง.
- ฟอสฟอรัส อันตรายมากกว่าอาหารจากสารเติมแต่งมากกว่าจากถั่วหรือเมล็ดพืช เพราะฟอสฟอรัสจากสารเติมแต่งอาจถูกดูดซึมได้ที่ 90–100%.
- แมกนีเซียม มักอยู่ที่ 1.7–2.2 mg/dL; อาหารที่มีแมกนีเซียมสูงช่วยสุขภาพเมตาบอลิซึมได้ แต่การเสริมอาหารอาจมีความเสี่ยงใน CKD ระยะรุนแรง.
- อัตราส่วนอัลบูมินต่อครีเอตินินในปัสสาวะ ต่ำกว่า 30 mg/g มักเป็นค่าปกติ, 30–300 mg/g เพิ่มขึ้นระดับปานกลาง และสูงกว่า 300 mg/g บ่งชี้ความเสี่ยงที่สูงขึ้นต่อไตและโรคหัวใจและหลอดเลือด.
อาหารสำหรับไตที่ปลอดภัยที่สุดเริ่มจาก “รูปแบบผลตรวจจริง” ของคุณ
การตรวจเลือดประจำปีที่ดี อาหารสำหรับโรคไต ปกป้องผลตรวจของคุณด้วยการจับคู่โปรตีน โซเดียม โพแทสเซียม และฟอสฟอรัสให้เข้ากับค่า eGFR ของคุณ โปรตีนในปัสสาวะ เกลือแร่ และยา—ไม่ใช่การห้ามอาหารชนิดเดียวกันสำหรับทุกคน ถ้าโพแทสเซียม 4.2 mmol/L ฟอสเฟต 3.6 mg/dL และค่า ACR ในปัสสาวะสูง ฉันมักจะกังวลเรื่องโซเดียมและความดันโลหิตมากกว่ากล้วย.

ฉันคือ Thomas Klein, MD และเมื่อฉันตรวจดูแผงผลไตใน คันเตสตี เอไอ, คำถามแรกไม่ใช่ “อาหารอะไรที่ไม่ดี?” แต่เป็นว่ารูปแบบนั้นดูเหมือนการกรองลดลง ภาวะขาดน้ำ ผลจากยา การรั่วของโปรตีน ภาระความเป็นกรด ความไม่สมดุลของแร่ธาตุ หรือเป็นเพียงผลเดี่ยวที่มีสัญญาณรบกวน—การ อาหารสำหรับโรคไต อ่านผลเริ่มจากตรงนั้น.
ณ วันที่ 29 เมษายน 2026 KDIGO กำหนดโรคไตเรื้อรังจากความผิดปกติของโครงสร้างหรือการทำงานของไตที่มีอยู่อย่างน้อย 3 เดือน รวมถึง eGFR ต่ำกว่า 60 มล./นาที/1.73 ตร.ม. หรือ ค่า ACR ในปัสสาวะ 30 mg/g หรือสูงกว่า (KDIGO, 2024) เงื่อนไขเรื่องเวลานี้สำคัญ; ฉันเคยเห็นผู้ป่วยที่กังวลปรับเปลี่ยนอาหารทั้งชุดหลังจากได้ผลครีเอตินินหลังออกกำลังกายเพียงครั้งเดียว ซึ่งกลับมาเป็นปกติในอีก 10 วันถัดมา.
กรอบคิดที่เป็นประโยชน์อย่างหนึ่ง: อาหารแทบไม่ “เพิ่ม eGFR” โดยตรงภายในหนึ่งสัปดาห์ แต่สามารถขยับตัวชี้วัดความเสี่ยงรอบ ๆ ค่า eGFR ได้ โซเดียมสามารถเปลี่ยนความดันโลหิตและภาวะอัลบูมินรั่ว โปรตีนสามารถทำให้ BUN เปลี่ยน คเนื้อสัตว์ที่ปรุงสุกสามารถดันครีเอตินิน โภชนาการโพแทสเซียมอาจทำให้การขับออกที่บกพร่องแสดงออก และสารเติมแต่งฟอสฟอรัสสามารถดัน PTH ได้ก่อนที่ผู้ป่วยจะรู้สึกอะไร.
สำหรับข้อมูลพื้นฐานเกี่ยวกับการกรองที่เปลี่ยนตามอายุ และเหตุผลที่การประเมินค่าเพียงครั้งเดียวอาจทำให้เข้าใจผิด our คู่มืออายุสำหรับ eGFR เป็นตัวอ่านประกอบที่ดี การปรับที่ทำได้จริงคือการเทียบแผงผลตรวจปัจจุบันของคุณกับผลครีเอตินินก่อนหน้า ถ้ามีให้ใช้ cystatin C ค่า ACR ค่า CO2 โพแทสเซียม ฟอสเฟต และความดันโลหิต—ไม่ใช่การทำตาม “อาหารสำหรับโรคไต” ที่ถ่ายเอกสารมาจากห้องรอ.
eGFR, ครีเอตินีน และซิสตาติน ซี บอกเรื่องโภชนาการที่ต่างกัน
การประเมิน eGFR คือการประเมินการกรอง ส่วนครีเอตินินและ cystatin C คือส่วนประกอบที่ใช้ในการประเมินนั้น. ครีเอตินินได้รับอิทธิพลอย่างมากจากมวลกล้ามเนื้อ การกินเนื้อสัตว์ และยาบางชนิด ขณะที่ cystatin C มีความสัมพันธ์กับกล้ามเนื้อน้อยกว่า แต่สามารถเปลี่ยนแปลงได้จากการอักเสบ การใช้สเตียรอยด์ และสถานะของไทรอยด์.

ค่า eGFR ที่คำนวณจากครีเอตินิน 58 mL/min/1.73 m² ไม่ได้หมายความเหมือนกันในนักเพาะกายอายุ 32 ปี กับผู้ที่อายุ 82 ปีที่มีน้ำหนักลด. คันเตสตี เอไอ เปรียบเทียบครีเอตินิน บริบทของร่างกาย BUN เกลือแร่ และผลตรวจในอดีต โดยใช้ our มาตรฐานการยืนยันทางคลินิก แทนที่จะรักษาสัญญาณนั้นเป็นการวินิจฉัย.
ครีเอตินินในเลือดมักอยู่ราว 0.6–1.1 mg/dL ในผู้หญิงผู้ใหญ่ และ 0.7–1.3 mg/dL ในผู้ชายผู้ใหญ่ แต่ช่วงค่าห้องแล็บจะแตกต่างตามวิธีการและประชากร. ห้องแล็บในยุโรพบางแห่งรายงานครีเอตินินเป็น µmol/L โดยที่ 1.0 mg/dL ประมาณ 88.4 µmol/L และการสลับหน่วยเกิดขึ้นบ่อยกว่าที่ผู้ป่วยคิด.
cystatin C อาจมีประโยชน์เมื่อครีเอตินินดูผิดสัดส่วนกับคนที่อยู่ตรงหน้าเรา ผู้ป่วยที่ร่างกายอ่อนแอซึ่งมีครีเอตินิน “ปกติ” 0.9 mg/dL อาจยังมีการกรองที่แท้จริงต่ำอยู่ ในขณะที่ผู้ป่วยที่มีกล้ามเนื้อมากซึ่งมีครีเอตินิน 1.4 mg/dL อาจมีค่า eGFR ที่อิงจาก cystatin C ซึ่งดูน่าเชื่อใจกว่า.
เมื่อ eGFR และครีเอตินินไม่สอดคล้องกัน ให้มองหาจังหวะของอาหารก่อนจะสันนิษฐานว่าการทำงานลดลง คู่มือของเราสำหรับ a GFR ต่ำแต่ creatinine ปกติ อธิบายว่าทำไมสมการจึงอาจทำให้เข้าใจผิดที่ขอบของอายุ มวลกล้ามเนื้อ และขนาดร่างกาย.
โปรตีนทำให้ค่า BUN เปลี่ยนเร็วกว่า eGFR
ปริมาณโปรตีนมีผลต่อ BUN โดยตรงที่สุด ไม่ใช่ eGFR. โดยทั่วไป BUN ในผู้ใหญ่จะอยู่ในช่วง 7–20 มก./ดล. และการเพิ่มขึ้นหลังสัปดาห์ที่กินโปรตีนสูงอาจสะท้อนการสร้างยูเรีย มากกว่าการบาดเจ็บไตอย่างฉับพลัน.

แนวทางโภชนาการปี 2020 ของ KDOQI แนะนำเป้าหมายโปรตีนแบบเฉพาะบุคคล รวมถึงประมาณ 0.55–0.60 กรัม/กก./วัน สำหรับผู้ใหญ่ที่ภาวะเมตาบอลิซึมคงที่และมี CKD ระยะ 3–5 ที่ไม่มีโรคเบาหวาน เมื่อได้รับการดูแล และ 0.6–0.8 กรัม/กก./วัน สำหรับผู้ใหญ่จำนวนมากที่มีโรคเบาหวานและ CKD (Ikizler et al., 2020) การฟอกไตต่างออกไป ผู้ป่วยฟอกไตจำนวนมากมักต้องการประมาณ 1.0–1.2 กรัม/กก./วัน เพราะการรักษาทำให้สูญเสียกรดอะมิโนเพิ่มขึ้น.
ผมเห็นรูปแบบนี้บ่อยมาก: ผู้ป่วยเริ่มกินผงโปรตีน 140 กรัม/วัน, BUN เพิ่มจาก 16 เป็น 31 มก./ดล., ครีเอตินินแทบไม่เปลี่ยน และค่า ACR ในปัสสาวะไม่เปลี่ยนเช่นกัน รูปแบบนี้ไม่เหมือนกับ eGFR ที่ลดลง แต่เป็นสัญญาณให้ถามว่าเป้าหมายโปรตีนเหมาะกับระยะไต น้ำหนักตัว ระดับการฝึก และความอยากอาหารหรือไม่.
อัตราส่วน BUN ต่อครีเอตินินที่สูงกว่า 20:1 มักบ่งชี้ภาวะขาดน้ำ การกินโปรตีนสูง ภาระไนโตรเจนจากทางเดินอาหาร หรือการไหลเวียนเลือดไปไตลดลง มากกว่าความเสียหายของไตโดยตรงจากตัวมันเอง. ของเรา คู่มือการแปลผล BUN ลงลึกถึงเหตุผลว่าทำไม BUN ถึงเป็นตัวชี้วัดที่ “มีสัญญาณรบกวน” เมื่ออ่านเพียงอย่างเดียว.
การปรับโปรตีนที่ปลอดภัยกว่ามักค่อยเป็นค่อยไป: ลดผงที่เกินก่อน แบ่งโปรตีนให้กระจายตลอดมื้อ และหลีกเลี่ยงการลดต่ำกว่าระดับที่ช่วยป้องกันการสูญเสียกล้ามเนื้อ ในผู้สูงอายุผมระมัดระวังเรื่องการจำกัดอย่างเข้มงวด เพราะภาวะกล้ามเนื้อน้อย (sarcopenia) อาจทำให้ครีเอตินินลดลงและทำให้ eGFR ดูดีขึ้นอย่างหลอกๆ.
ครีเอตินีนอาจสูงขึ้นจากการกินเนื้อสัตว์ การเสริมครีเอทีน และการฝึกหนัก
ครีเอตินินอาจเพิ่มขึ้นได้ด้วยเหตุผลที่ไม่ได้เกี่ยวกับความเสียหายของไตแบบถาวรโดยตรง. เนื้อสัตว์ที่ปรุงสุก อาหารเสริมครีเอตินิน ภาวะขาดน้ำ การออกกำลังกายแบบต้านทานหนัก และยาบางชนิด เช่น trimethoprim ล้วนทำให้ครีเอตินินเพิ่มขึ้นหรือทำให้ eGFR ที่คำนวณได้ลดลงชั่วคราวได้.

นักปั่นจักรยานวัย 41 ปีเคยอัปโหลดผลตรวจหลังจบการแข่งขันสุดสัปดาห์: ครีเอตินิน 1.38 mg/dL, eGFR 61 mL/min/1.73 m², BUN 28 mg/dL และ CK สูงเล็กน้อย หลังดื่มน้ำชุ่มและพัก 3 วันโดยไม่ฝึกหนัก ครีเอตินินกลับมาเป็น 1.08 mg/dL; นั่นคือเหตุผลว่าทำไม “บริบท” ถึงสำคัญกว่าความตื่นตระหนก.
ครีเอตินินถูกสร้างจากครีเอทีนในกล้ามเนื้อ ดังนั้นมวลกล้ามเนื้อที่มากขึ้นและการสลายตัวของกล้ามเนื้อเมื่อไม่นานมานี้อาจทำให้ผลตรวจสูงขึ้นได้. การตรวจซ้ำที่ “สะอาดที่สุด” มักทำหลัง 24–48 ชั่วโมงที่ไม่ออกกำลังกายหนัก และไม่กินอาหารมื้อใหญ่ที่มีเนื้อสัตว์ปรุงสุกมากในคืนก่อน โดยเฉพาะถ้าผลจะเป็นตัวตัดสินว่าต้องส่งต่อหรือไม่.
ครีเอทีนโมโนไฮเดรตไม่ได้ทำให้ไตเป็นพิษโดยอัตโนมัติในผู้ใหญ่ที่สุขภาพดี แต่ในโรคไตเรื้อรัง (CKD) จะทำให้การแปลผลซับซ้อน เพราะมันอาจเพิ่มการสร้างครีเอตินิน หาก eGFR ของคุณอยู่ในช่วงใกล้ขอบ ช่วงครีเอตินีนของเรา อธิบายว่าเมื่อใดที่ cystatin C หรือค่า ACR ในปัสสาวะอาจช่วยทำให้เรื่องชัดเจนขึ้น.
อย่า “โหลดน้ำ” อย่างหนักก่อนตรวจซ้ำ แต่อย่ามากเกินไป การให้น้ำมากเกินอาจทำให้โซเดียมและอัลบูมินเจือจาง ในขณะที่การให้น้ำตามปกติ—ปัสสาวะใสถึงเหลืองอ่อน ไม่อาเจียนหรือท้องเสีย—มักเพียงพอสำหรับการตรวจเคมีไตที่ยุติธรรม.
โซเดียมส่งผลต่อความเสี่ยงของไตผ่านความดันและโปรตีนในปัสสาวะ
โซเดียมเป็นหนึ่งในการเปลี่ยนแปลงด้านอาหารที่เกี่ยวข้องกับผลตรวจในห้องแล็บมากที่สุดใน CKD เพราะมันสามารถลดความดันโลหิตและลดอัลบูมินในปัสสาวะได้. โดยทั่วไปโซเดียมในเลือดจะคงอยู่ที่ 135–145 mmol/L ดังนั้นประโยชน์ต่อไตมักเห็นได้จากความดันโลหิตและ ACR มากกว่าจากผลโซเดียมในเลือดโดยตรง.

KDIGO และคลินิกโรคไตหลายแห่งมักตั้งเป้าการบริโภคโซเดียมให้น้อยกว่าประมาณ 2,000 mg/วัน ในผู้ป่วย CKD ที่มีความดันโลหิตสูง แม้ว่าในผู้สูงอายุที่เปราะบาง เหงื่อออกมาก และคนที่โซเดียมต่ำอยู่แล้ว อาจต้องได้รับคำแนะนำเฉพาะบุคคล อาหารโซเดียมต่ำที่ทำให้เวียนศีรษะ ล้ม หรือทำให้โซเดียมเหลือ 130 mmol/L ไม่ใช่ชัยชนะ.
การ อาหาร DASH สำหรับความดันโลหิต มีพลังมาก แต่ผู้ป่วยโรคไตอาจต้องใช้เวอร์ชันที่ปรับแล้ว เพราะ DASH มาตรฐานมีโพแทสเซียมและอาหารที่มีฟอสฟอรัสสูง ในการทดลอง DASH-Sodium การผสมผสานการกินแบบ DASH กับโซเดียมต่ำทำให้ความดันโลหิตซิสโตลิกลดลงประมาณ 7.1 mmHg ในผู้ใหญ่ที่ไม่มีความดันสูง และ 11.5 mmHg ในผู้ใหญ่ที่มีความดันสูง เมื่อเทียบกับอาหารควบคุมที่มีโซเดียมสูง (Sacks et al., 2001).
Albuminuria คือจุดที่โซเดียมน่าสนใจ เมื่อการกินโซเดียมสูง ยากลุ่ม ACE inhibitors และ ARBs มักลดโปรตีนในปัสสาวะได้น้อยลงอย่างมีประสิทธิภาพ; เมื่อโซเดียมลดลง ยาเดิมอาจดู “แรงกว่า” ในค่า ACR รอบถัดไป.
ถ้าค่าที่บ้านของคุณสูง ให้เทียบกับเทคนิคที่เป็นมาตรฐานก่อนจะโทษมื้อเย็นของคุณ Our คู่มือช่วงความดันโลหิต อธิบายว่าทำไมขนาดผ้าพันแขน เวลาพัก และช่วงเวลาที่กินยาตอนเช้าถึงสามารถทำให้ตัวเลขเปลี่ยนได้ถึง 10 mmHg.
อาหารที่มีโพแทสเซียมสูงไม่ได้ถูกห้ามเสมอไป
อาหารที่มีโพแทสเซียมสูงจำเป็นต้องจำกัดก็ต่อเมื่อรูปแบบผลตรวจของคุณบ่งชี้ความเสี่ยงต่อการคั่งของโพแทสเซียมในร่างกาย. โพแทสเซียม 3.8 mmol/L ในผู้ที่ใช้ยาขับปัสสาวะกลุ่ม thiazide เป็นปัญหาคนละแบบกับโพแทสเซียม 5.7 mmol/L ในผู้ที่ใช้ spironolactone โดยมี eGFR 28.
โดยทั่วไปโพแทสเซียมในซีรัมอยู่ในช่วง 3.5–5.0 mmol/L และค่าที่สูงกว่า 5.5 mmol/L มักควรได้รับการทบทวนอย่างรวดเร็ว. ผล 6.0 mmol/L หรือสูงกว่าสามารถเป็นภาวะเร่งด่วนได้ โดยเฉพาะเมื่อมีอ่อนแรง ใจสั่น การเปลี่ยนแปลงของ ECG โรคไตเรื้อรังระยะลุกลาม หรือยาที่เพิ่มโพแทสเซียม.
สาเหตุที่พบบ่อย อาหารที่มีโพแทสเซียมสูง ได้แก่ กล้วย ส้ม มันฝรั่ง มะเขือเทศ ผักโขม อะโวคาโด ผลไม้แห้ง ถั่ว และน้ำมะพร้าว ข้อควรระวังคือ โพแทสเซียมจากพืชทั้งส่วนมักถูกดูดซึมได้ไม่สมบูรณ์เท่าโพแทสเซียมเกลือในอาหารเสริม รวมถึงสารทดแทนเกลือโซเดียมต่ำและอาหารแปรรูป.
ฉันเคยเห็นผู้ป่วยหยุดผลไม้และผักแทบทั้งหมดหลังจากโพแทสเซียมครั้งหนึ่งอยู่ที่ 5.2 mmol/L แล้วกลับมาท้องผูก เป็นกรด และทรมาน ก่อนทำแบบนั้น ให้ตรวจดูภาวะเม็ดเลือดแดงแตก (hemolysis) ในตัวอย่าง การเปลี่ยนแปลงยาล่าสุด สารทดแทนเกลือ trimethoprim ยากลุ่ม NSAIDs ยากลุ่ม ACE inhibitors ยากลุ่ม ARBs spironolactone และว่าการเจาะเลือดทำได้ยากหรือไม่.
สำหรับผู้ป่วยที่จำเป็นต้องลดจริง ๆ ขนาดส่วนและวิธีการปรุงอาหารช่วยได้ เรา คู่มือช่วงโพแทสเซียม ครอบคลุมการแช่/ชะล้างมันฝรั่ง การหลีกเลี่ยงเกลือโพแทสเซียมคลอไรด์ และการเฝ้าดูแนวโน้มหลังจากมีการปรับเปลี่ยน.
โพแทสเซียม, CO2 และคลอไรด์อธิบายได้มากขึ้นเมื่อพิจารณาร่วมกัน
การตัดสินใจเรื่องอาหารสำหรับไตจะปลอดภัยขึ้นเมื่ออ่านโพแทสเซียมร่วมกับ CO2 คลอไรด์ และโซเดียม. CO2 ต่ำอาจบ่งชี้ภาวะกรดเมตาบอลิก ซึ่งส่งผลต่อความทนต่อโปรตีน ความเสี่ยงด้านกระดูกและแร่ธาตุ และปริมาณอาหารจากพืชที่ผู้ป่วยสามารถใช้ได้อย่างปลอดภัย.

ค่า CO2 ในเลือด (serum CO2) จากการตรวจเคมีพื้นฐาน (basic metabolic panel) มักสะท้อนถึงไบคาร์บอเนต และโดยมากอยู่ในช่วง 22–29 mmol/L. ในโรคไตเรื้อรัง (CKD) ค่า CO2 ต่ำกว่า 22 mmol/L อาจบ่งชี้ภาวะกรดเมตาบอลิก ซึ่งสัมพันธ์กับการสูญเสียกล้ามเนื้อ การทำหน้าที่บัฟเฟอร์ของกระดูก และการเสื่อมของไตที่เร็วขึ้นในบางกลุ่มตัวอย่าง.
นี่คือรูปแบบที่ฉันไม่มองข้าม: โพแทสเซียม 5.3 mmol/L, คลอไรด์ 111 mmol/L, CO2 18 mmol/L และ eGFR 34 mL/min/1.73 m² ชุดค่านี้อาจทำให้ “อาหารแนวด่าง” ที่กินผลไม้มากดูน่าสนใจในเชิงทฤษฎี แต่ความเสี่ยงของโพแทสเซียมทำให้แพทย์อาจพิจารณาการรักษาด้วยไบคาร์บอเนต การทบทวนยาที่ใช้อยู่ หรือเลือกอาหารที่มีโพแทสเซียมต่ำอย่างเหมาะสมแทน.
โครงข่ายประสาทของ Kantesti จัดกลุ่มอิเล็กโทรไลต์เป็นรูปแบบแทนที่จะอ่านเป็นสัญญาณเตือนแยกเดี่ยว หากคุณอยากรู้พื้นฐานก่อน เรา แนวทางตรวจอิเล็กโทรไลต์ อธิบายว่าโซเดียม โพแทสเซียม คลอไรด์ และ CO2 ชี้ไปที่ภาวะขาดน้ำ ความผิดปกติของกรด-ด่าง หรือผลจากยาได้อย่างไร.
อย่าใช้เบกกิ้งโซดาด้วยตัวเองหากคุณมีความดันโลหิตสูง บวม หรือหัวใจล้มเหลว ช้อนชา 1 ช้อนมีโซเดียมประมาณ 1,200 mg, ซึ่งมากพอที่จะทำให้แผนอาหารสำหรับไตที่เน้นโซเดียมต่ำอย่างรอบคอบเสียไป.
อาหารที่มีแมกนีเซียมสูงอาจช่วยได้ แต่การเสริมอาหารต้องระวัง
อาหารที่มีแมกนีเซียมสูงมักปลอดภัยกว่าการเสริมแมกนีเซียมใน CKD แต่โรคไตระยะลุกลามจะทำให้ “ขอบเขต” แคบลง. โดยทั่วไปค่าแมกนีเซียมในเลือด (serum magnesium) มักอยู่ที่ 1.7–2.2 mg/dL และระดับที่สูงกว่าประมาณ 2.6 mg/dL มักบ่งชี้การคั่งหรือการได้รับมากเกินในหลายห้องแล็บ.

อาหารที่อุดมด้วยแมกนีเซียม ได้แก่ เมล็ดฟักทอง อัลมอนด์ เม็ดมะม่วงหิมพานต์ ถั่วต่าง ๆ ถั่วเลนทิล ผักโขม ดาร์กช็อกโกแลต และธัญพืชไม่ขัดสี แต่อาหารกลุ่มเดียวกันอาจมีโพแทสเซียมหรือฟอสฟอรัสด้วย ดังนั้นขนาดที่เหมาะสมขึ้นอยู่กับฟอสเฟต โพแทสเซียม พฤติกรรมการขับถ่าย สถานะโรคเบาหวาน และระยะของ eGFR.
หลักฐานเกี่ยวกับแมกนีเซียมและ CKD นั้นค่อนข้างปนกันจริง ๆ แมกนีเซียมต่ำสัมพันธ์กับภาวะดื้อต่ออินซูลิน ความเสี่ยงต่อภาวะหัวใจเต้นผิดจังหวะ และการกลายเป็นหินปูนในหลอดเลือดจากงานสังเกต แต่การเสริมอาจสะสมได้เมื่อ eGFR ต่ำ โดยเฉพาะเมื่อใช้ยาระบายหรือยาลดกรดที่มีแมกนีเซียม.
ฉันสบายใจกับแนวทาง “เน้นอาหารก่อน” สำหรับแมกนีเซียมมากกว่า เมื่อโพแทสเซียมปกติและควบคุมฟอสเฟตได้ เรา คู่มือช่วงแมกนีเซียม อธิบายว่าทำไมแมกนีเซียมในเลือดที่ “ปกติ” ยังอาจพลาดการพร่องภายในเซลล์ โดยเฉพาะในคนที่ใช้ PPIs หรือยาขับปัสสาวะแบบลูป.
เช็กลิสต์ที่ทำได้จริง: หาก eGFR ต่ำกว่า 30 mL/min/1.73 m² ให้ปรึกษาก่อนรับประทานแมกนีเซียมไกลซิเนต ซิเตรต หรือออกไซด์ ความเป็นพิษของแมกนีเซียมอาจทำให้ความดันโลหิตต่ำ รีเฟล็กซ์ช้าลง ง่วงซึม และมีปัญหาเรื่องจังหวะการเต้นของหัวใจเมื่อระดับสูงขึ้นอย่างมีนัยสำคัญ.
สารเติมแต่งฟอสฟอรัสทำให้ผลตรวจเปลี่ยนมากกว่าถั่ว
ฟอสฟอรัสจากสารเติมแต่งมักรบกวนผลตรวจในห้องแล็บมากกว่าฟอสฟอรัสที่ติดอยู่ตามธรรมชาติในอาหารจากพืช. โดยทั่วไปฟอสฟอรัสในเลือด (serum phosphorus) มักอยู่ที่ 2.5–4.5 mg/dL แต่ PTH และ FGF23 อาจเพิ่มขึ้นก่อนที่ฟอสฟอรัสจะออกจากช่วงอ้างอิง.

นี่คือส่วนที่ผู้ป่วยมักไม่ค่อยได้ยิน: ฟอสฟอรัสในเครื่องดื่มโคล่า เนื้อสัตว์แปรรูป ขนมอบที่เก็บได้นาน และอาหารบรรจุแบบ “เสริมคุณค่า” อาจถูกดูดซึมที่ 90–100%, ในขณะที่ฟอสฟอรัสจากไฟเตตในพืชมักถูกดูดซึมน้อยกว่ามาก ดังนั้นแกงถั่วกับมื้ออาหารที่ใส่ฟอสเฟตแบบแปรรูปอาจให้ผลต่อผลตรวจในห้องแล็บที่แตกต่างกันมาก แม้ฉลากจะดูคล้ายกันก็ตาม.
ฟอสฟอรัสสูงในโรคไตเรื้อรัง (CKD) เชื่อมโยงกับภาวะพาราไทรอยด์ทำงานเกินทุติยภูมิ ความเสี่ยงการกลายเป็นหินปูนในหลอดเลือด และปัญหาการหมุนเวียนของกระดูก หากผล PTH ค่อยๆ สูงขึ้นโดยที่แคลเซียมและฟอสฟอรัสยังปกติ อาจเป็นสัญญาณเริ่มต้นของความผิดปกติแร่ธาตุ-กระดูก ไม่ใช่เหตุผลที่จะตัดโปรตีนทั้งหมดแบบสุ่มๆ.
ฉลากอาหารทำให้หงุดหงิด เพราะมักไม่ระบุฟอสฟอรัสเป็นมิลลิกรัมเสมอไป ให้มองหาคำในส่วนประกอบที่มี “phos” แล้วจับคู่กับผลตรวจ renal panel ของคุณ; our คู่มือการตรวจเลือด PTH อธิบายว่ แคลเซียม วิตามินดี ฟอสเฟต และ PTH เข้ากันอย่างไร.
ฉันมักให้ผู้ป่วยหยุดสารเติมแต่งฟอสเฟตเป็นเวลา 4–6 สัปดาห์ก่อนเราจะลดอาหารทั้งชนิดที่ดีต่อสุขภาพเพียงอย่างเดียว การเปลี่ยนแปลงครั้งเดียวนี้สามารถลดภาระฟอสฟอรัสได้ โดยไม่ทำให้การกินใยอาหารทนลง ท้องผูก คอเลสเตอรอล หรือการคุมระดับน้ำตาลแย่ลง.
โปรตีนในปัสสาวะมักตอบสนองต่อโซเดียมและความดันก่อนเป็นอันดับแรก
อัลบูมินในปัสสาวะเป็นหนึ่งในตัวชี้วัดความเสี่ยงของไตที่ตอบสนองต่ออาหารได้มาก โดยเฉพาะผ่านโซเดียมและความดันโลหิต. ACR ต่ำกว่า 30 mg/g โดยทั่วไปปกติ, 30–300 mg/g เพิ่มขึ้นปานกลาง และสูงกว่า 300 mg/g เพิ่มขึ้นอย่างรุนแรง.

เมื่อฉันเห็น eGFR 72 mL/min/1.73 m² ร่วมกับ ACR 420 mg/g ฉันไม่ได้เรียกว่าไต “ปกติดี” แค่เพราะครีเอตินินปกติ ภาวะอัลบูมินรั่วทำนายความเสี่ยงต่อไตและโรคหัวใจและหลอดเลือด และมักดีขึ้นเมื่อปริมาณโซเดียมลดลง ความดันโลหิตดีขึ้น และการรักษาโรคเบาหวานเข้มงวดขึ้น.
ปริมาณโปรตีนมีความสำคัญ แต่แหล่งที่มาของโปรตลีก็สำคัญเช่นกัน รูปแบบโปรตีนที่เน้นพืชอาจลดภาระกรดและช่วยให้ความดันโลหิตดีขึ้น ในขณะที่อาหารที่มีโปรตีนจากสัตว์สูงมากอาจเพิ่มความเครียดด้านการไหลเวียนของเลือดในไตในผู้ป่วยที่มีความเสี่ยง ผลของมันแตกต่างกัน และแพทย์มีความเห็นไม่ตรงกันว่าจะเข้มงวดแค่ไหนใน CKD ระยะเริ่มต้น.
อัลบูมินในซีรัมโดยปกติมักอยู่ช่วง 3.5–5.0 g/dL และอัลบูมินในซีรัมต่ำร่วมกับโปรตีนในปัสสาวะสูงอาจบ่งชี้การสูญเสียโปรตีนในปัสสาวะอย่างมีนัยสำคัญ. ของเรา คู่มืออัลบูมินต่ำ อธิบายว่าทำไมอาการบวม โรคตับ ภาวะอักเสบ และการสูญเสียการทำงานของไตจึงต้องแยกพิจารณา.
เคล็ดลับที่ใช้ได้จริง: ทำการตรวจ ACR ซ้ำจากปัสสาวะช่วงเช้าแรกเมื่อทำได้ การออกกำลังกาย ไข้ การติดเชื้อทางเดินปัสสาวะ การมีประจำเดือน ภาวะน้ำตาลสูงมาก และตัวอย่างที่เจือจางมาก ล้วนทำให้การตีความโปรตีนในปัสสาวะยากขึ้น.
รูปแบบ DASH สามารถเป็นมิตรกับไตได้หลังปรับเปลี่ยน
อาหาร DASH เพื่อความดันโลหิตช่วยผู้ป่วย CKD ได้ แต่ DASH มาตรฐานไม่ได้ปลอดภัยโดยอัตโนมัติสำหรับทุกคนที่มี eGFR ลดลง. ปริมาณผลไม้ ผัก ถั่ว และพืชตระกูลถั่วที่สูง อาจทำให้ผู้ป่วยที่ขับออกได้ไม่ดีมีโพแทสเซียมหรือฟอสฟอรัสเพิ่มขึ้น.

ใน CKD ระยะเริ่มต้นที่โพแทสเซียมปกติ รูปแบบ DASH มักมีเหตุผลทางสรีรวิทยา: โซเดียมต่ำขึ้น ใยอาหารมากขึ้น ไขมันไม่อิ่มตัวมากขึ้น และความดันโลหิตดีขึ้น ใน CKD ระยะ 4 ที่โพแทสเซียม 5.6 mmol/L แผนมื้อนี้อาจต้องลดผักที่มีโพแทสเซียมลง ลดสัดส่วนถั่วตระกูลถั่ว และหลีกเลี่ยงเกลือทดแทน.
สิ่งสำคัญคือ DASH เป็น “รูปแบบ” ไม่ใช่คำสั่งให้กินอาหารที่มีโพแทสเซียมสูงที่สุดทุกวัน คุณยังคงโครงสร้างที่ช่วยลดโซเดียมได้ โดยเลือกแอปเปิลแทนน้ำส้ม เลือกข้าวหรือพาสต้าแทนมันฝรั่ง และเลือกอาหารสดที่ไม่ใส่เกลือฟอสเฟตแทนอาหารบรรจุที่เติมฟอสเฟต.
ผู้ป่วยโรคเบาหวานจะมีชั้นพิเศษเพิ่มขึ้น หาก HbA1c สูง การคุมระดับน้ำตาลสามารถลดความเสี่ยงของภาวะอัลบูมินรั่วในปัสสาวะได้ และของเรา คู่มือการตรวจเลือดเบาหวาน อธิบายว่าทำไมควรอ่าน HbA1c น้ำตาลขณะอดอาหาร และตัวชี้วัดไตไปพร้อมกัน.
การตรวจประจำของผมดูน่าเบื่อแต่มีประโยชน์: เปลี่ยนตัวแปรด้านอาหารอย่างใดอย่างหนึ่งเป็นเวลา 2–4 สัปดาห์ แล้วค่อยตรวจซ้ำในห้องแล็บที่มีแนวโน้มจะเปลี่ยนมากที่สุด ถ้าคุณเปลี่ยนทั้งโซเดียม โพแทสเซียม โปรตีน และอาหารเสริมพร้อมกันทีเดียว จะไม่มีใครบอกได้ว่า “คันโยก” ไหนช่วยจริง.
ยาสามารถเปลี่ยนสิ่งที่นับว่าเป็น “อาหารที่ปลอดภัย”
คำแนะนำเรื่องอาหารสำหรับไตจะเปลี่ยนไปเมื่อยาปรับโพแทสเซียม โซเดียม ครีเอตินิน หรือสมดุลกรด-เบส. ยากลุ่ม ACE inhibitors, ARBs, สไปโรโนแลคโตน, ยากลุ่ม SGLT2 inhibitors, ยาขับปัสสาวะ, NSAIDs, ไตรเมโธพริม และยาจับฟอสเฟต ล้วนสามารถเปลี่ยนวิธีที่อาหารสะท้อนออกมาในผลตรวจแล็บได้.

ACE inhibitors และ ARBs อาจทำให้ครีเอตินินสูงขึ้นเล็กน้อยหลังเริ่มยา ซึ่งมักยอมรับได้ถึงประมาณ 30% หากโพแทสเซียมยังอยู่ในระดับปลอดภัย และผู้ป่วยมีความคงที่ทางคลินิก การเพิ่มขึ้นเล็กน้อยของครีเอตินินอาจสะท้อนถึงความดันในโกลเมอรูลัสที่ลดลง ซึ่งอาจช่วยปกป้องไตได้เมื่อมีภาวะอัลบูมินรั่วในปัสสาวะ.
สไปโรโนแลคโตนและอีพลีเรโนนคือจุดที่รายการอาหารที่มีโพแทสเซียมเริ่มมีความสำคัญมากขึ้น ผู้ป่วยที่กินอาหารที่มีโพแทสเซียมสูงอาจทำได้ดีจนกว่าจะมีการเพิ่มยาที่ช่วยสงวนโพแทสเซียม แล้วการใช้น้ำสลัดทดแทนเกลือที่มีโพแทสเซียมคลอไรด์อาจทำให้ผลแล็บพุ่งจาก 4.8 เป็น 6.1 mmol/L ได้อย่างรวดเร็ว.
NSAIDs เป็นปัญหาเงียบๆ การกินไอบูโพรเฟนระหว่างภาวะขาดน้ำ เจ็บป่วย หรือออกกำลังกายหนัก อาจลดการไหลเวียนเลือดไปที่ไต ทำให้ครีเอตินินสูงขึ้น และทำให้แผนเรื่องโปรตีนหรือโซเดียมที่โดยปกติสมเหตุสมผลดูเหมือนเป็นอันตราย.
อาหารเสริมควรได้รับความเคารพเทียบเท่ากับยาที่ต้องสั่งโดยแพทย์ ของเรา คู่มือเวลาการกินอาหารเสริม ครอบคลุมเรื่องปฏิกิริยาระหว่างกัน และสำหรับผู้ป่วยโรคไต ผมจะถามโดยเฉพาะเกี่ยวกับครีเอทีน แมกนีเซียม โพแทสเซียม วิตามินซีขนาดสูง สารสกัดขมิ้น และส่วนผสมสำหรับเพาะกาย.
ควรนัดตรวจซ้ำเพื่อมาตอบคำถามเดียว
การตรวจแล็บไตซ้ำที่ดีที่สุดควรจัดเวลาให้ตรงกับการเปลี่ยนอาหารเฉพาะที่คุณทำ. BUN อาจเปลี่ยนภายในไม่กี่วันหลังปรับโปรตีน โพแทสเซียมอาจเปลี่ยนภายใน 24–72 ชั่วโมงหลังตัวกระตุ้นครั้งใหญ่ และ ACR มักต้องใช้เวลาหลายสัปดาห์เพื่อให้ความดันโลหิตและปริมาณโซเดียมคงที่ขึ้น.

หากกังวลเรื่องครีเอตินิน ให้ตรวจซ้ำหลังดื่มน้ำตามปกติ ไม่ออกกำลังกายหนัก 24–48 ชั่วโมง และไม่กินอาหารมื้อเย็นที่เป็นเนื้อสัตว์ปรุงสุกปริมาณมากในคืนก่อนหน้า หากกังวลเรื่องโพแทสเซียม ให้ตรวจซ้ำเร็วขึ้นหลังหยุดเกลือโพแทสเซียมคลอไรด์หรืออาหารเสริมที่มีความเสี่ยง โดยเฉพาะเมื่อ eGFR ต่ำกว่า 45 mL/min/1.73 m².
สำหรับปัสสาวะ ACR ผมชอบดูตัวอย่างที่ผิดปกติ 2 ใน 3 ก่อนจะกล่าวอ้างใหญ่ๆ เว้นแต่ค่าจะสูงมากหรือภาพทางคลินิกชัดเจน ACR สามารถแกว่งได้จากการติดเชื้อ การออกกำลังกาย ไข้ ภาวะน้ำตาลพุ่ง และแม้แต่ช่วงเวลาที่เก็บตัวอย่าง.
Kantesti AI อ่านแนวโน้มจากไฟล์ PDF และรูปภาพที่อัปโหลด ไม่ใช่แค่ค่าสูงๆ ต่ำๆ ที่แยกเดี่ยว ของเรา เครื่องมือประวัติผลตรวจเลือด ช่วยให้ผู้ป่วยเห็นว่าครีเอตินินเปลี่ยนจาก “สัญญาณรบกวน” 0.05 mg/dL หรือเปลี่ยนด้วยแนวโน้มที่มีความหมายทางคลินิก.
จดบันทึกง่ายๆ 7 วันก่อนตรวจแล็บซ้ำ: ปริมาณโปรตีนเป็นกรัมหากคุณติดตาม อาหารร้านที่ผิดปกติ การใช้น้ำสลัดทดแทนเกลือ อาหารเสริม การออกกำลังกาย ท้องเสีย อาเจียน และยาตัวใหม่ บันทึกนั้นมักอธิบายผลได้เร็วกว่าอีกหนึ่งการตรวจที่มีค่าใช้จ่ายสูง.
รูปแบบผลตรวจบางอย่างไม่ควรรอให้ลองปรับอาหาร
การเปลี่ยนอาหารยังไม่พอเมื่อผลตรวจไตบ่งชี้ความเสี่ยงเร่งด่วน. โพแทสเซียม 6.0 mmol/L ขึ้นไป ครีเอตินินที่สูงขึ้นอย่างรวดเร็ว ภาวะกรดรุนแรง โซเดียมต่ำมาก อาการบวมร่วมกับอัลบูมินต่ำ หรืออาการต่างๆ เช่น เจ็บหน้าอก สับสน หรืออ่อนแรงรุนแรง ต้องได้รับคำแนะนำทางการแพทย์อย่างรวดเร็ว.

ครีเอตินินเพิ่มขึ้น 0.3 mg/dL ภายใน 48 ชั่วโมง อาจเข้าเกณฑ์ภาวะไตบาดเจ็บเฉียบพลันได้ในสถานการณ์ทางคลินิกที่เหมาะสม. นี่แตกต่างอย่างมากจากการเพิ่มขึ้นอย่างช้าๆ ในช่วงหลายปี และไม่ควรจัดการด้วยการกินโปรตีนน้อยลงเพียงอย่างเดียว.
อาการของโพแทสเซียมอาจคลุมเครือหรือไม่มีอาการก็ได้ ผมเคยเห็นผู้ป่วยที่มีโพแทสเซียม 6.4 mmol/L รู้สึก “ค่อนข้างเหนื่อย” แค่นั้น และไม่มีอะไรเพิ่มเติม นี่จึงเป็นเหตุผลว่าทำไมภาวะโพแทสเซียมสูงถึงต้องให้ความสำคัญอย่างจริงจัง แม้ผู้ป่วยจะดูปกติดีก็ตาม.
โซเดียมต่ำมากก็เป็นอีกกับดักหนึ่ง หากโซเดียมต่ำกว่า 130 mmol/L การดื่มน้ำเพิ่มเพราะ “ไตต้องการล้าง” อาจทำให้แย่ลง; ของเรา แนวทางโซเดียมต่ำ อธิบายว่าทำไมต้องจัดการให้ถูกต้องก่อนเรื่องการเจือจาง ยา และฮอร์โมน.
ใช้อาหารเป็นตัวช่วยระยะยาว ไม่ใช่การรักษาฉุกเฉิน หากรายงานแล็บระบุว่า “วิกฤต” หรือผู้ป่วยมีอาการหายใจลำบาก เป็นลม อาการเจ็บหน้าอก อาเจียนรุนแรง หรือมีความสับสนใหม่ การดูแลทางคลินิกต้องมาก่อนการวางแผนเรื่องอาหาร.
Kantesti เชื่อมโยงผลตรวจไตกับการตัดสินใจเรื่องอาหารอย่างไร
Kantesti เชื่อมโยงโภชนาการสำหรับไตเข้ากับรูปแบบผลแล็บทั้งหมด: eGFR, ครีเอตินีน, BUN, อิเล็กโทรไลต์, CO2, แคลเซียม, ฟอสเฟต, อัลบูมิน และตัวชี้วัดในปัสสาวะ. AI ของเราจะไม่บอกผู้ป่วยโรคไตทุกคนให้หลีกเลี่ยงอาหารชนิดเดียวกัน มันจะมองหาข้อจำกัดที่ “ปรากฏจริง” ในข้อมูล.

แพลตฟอร์มของเราสามารถอ่าน PDF หรือรูปภาพผลตรวจแล็บได้ภายในประมาณ 60 วินาที และแปลผลให้เป็นรูปแบบที่เข้าใจง่าย หากคุณอยากลองกับแผงตรวจไตของคุณเอง ให้ใช้ของเรา คำแนะนำทางการแพทย์ในวันเดียวกันมีเหตุผลสำหรับกรณีที่มีไข้ร่วมกับนิวโทรฟิลต่ำมาก อาการแย่ลงอย่างรวดเร็ว สับสน มีปัญหาในการหายใจ หรือ CBC ที่ผิดปกติในมากกว่าหนึ่งสายเซลล์ แพทย์ใน และรวมค่า ACR ในปัสสาวะหรือการตรวจปัสสาวะ หากคุณมี.
Kantesti AI อ่านผลตัวบ่งชี้มากกว่า 15,000 รายการ ครอบคลุมเคมีในเลือด แผงตรวจไต ตัวชี้วัดในปัสสาวะ การตรวจเมตาบอลิซึม และสารอาหารรอง สำหรับผู้ป่วยที่ต้องการทำความเข้าใจชื่อของตัวบ่งชี้ก่อนอัปโหลด ให้ของเรา biomarker guide อธิบายคำย่อที่มักปรากฏในรายงานเกี่ยวกับไต.
ผมยังบอกผู้ป่วยเหมือนที่ผมพูดในคลินิก: การอ่านผลด้วย AI ไม่ใช่การแทนที่แพทย์โรคไต แพทย์เวชปฏิบัติทั่วไป หรือผู้เชี่ยวชาญด้านโภชนาการสำหรับโรคไตของคุณ เป็นวิธีในการจับรูปแบบ เตรียมคำถามได้ดีขึ้น และหลีกเลี่ยงความผิดพลาดแบบคลาสสิกของการจำกัดโพแทสเซียม โปรตีน หรือฟอสฟอรัสโดยไม่มีหลักฐาน.
ทีมแพทย์ของ Kantesti ได้รับการอธิบายไว้ใน คณะกรรมการที่ปรึกษาทางการแพทย์, และข้อมูลพื้นฐานของบริษัทมีให้ที่ เกี่ยวกับคันเตสตี. Thomas Klein, MD ทบทวนเนื้อหาที่เกี่ยวข้องกับไตด้วยอคติแบบเดียวกับที่ผมใช้ในการรักษาทางคลินิก: ปกป้องผู้ป่วยก่อน แล้วค่อยปรับตัวเลขให้เหมาะสม.
บันทึกงานวิจัย การตรวจสอบความถูกต้อง และสิ่งที่เรายังไม่รู้
หลักฐานสำหรับอาหารสำหรับโรคไตแข็งแรงที่สุดในเรื่องการลดโซเดียม การควบคุมความดันโลหิต การลดภาวะอัลบูมินในปัสสาวะ และเป้าหมายโปรตีนที่มีการดูแล. หลักฐานยังอ่อนกว่าสำหรับการจำกัดโพแทสเซียมแบบครอบจักรวาล การจำกัดฟอสฟอรัสอย่างเข้มงวดในระยะเริ่มต้นของ CKD และการแก้ไขแร่ธาตุด้วยอาหารเสริมโดยไม่ยืนยันด้วยผลตรวจแล็บ.
Kantesti LTD. (2026). Clinical Validation Framework v2.0. Zenodo. ลิงก์ DOI. นอกจากนี้ยังสามารถดูได้ผ่าน ค้นหาใน ResearchGate และ การค้นหาใน Academia.edu.
Kantesti LTD. (2026). AI วิเคราะห์ผลเลือด: วิเคราะห์ 2.5M การตรวจ | รายงานสุขภาพโลก 2026. Zenodo. ลิงก์ DOI. นอกจากนี้ยังสามารถดูได้ผ่าน บันทึก ResearchGate และ บันทึก Academia.edu.
สำหรับเกณฑ์มาตรฐานเชิงเทคนิคที่กว้างขึ้น เครื่องมือ AI ของเรายังได้รับการประเมินในชุดข้อมูลตรวจสอบความถูกต้องระดับประชากรที่ลงทะเบียนไว้ล่วงหน้า ครอบคลุมหลายสาขา วิธีการมีอยู่ใน การประเมินมาตรฐานของเครื่องมือ AI. สิ่งนี้ไม่ได้ขจัดความไม่แน่นอนจากโภชนาการสำหรับไต แต่ทำให้กระบวนการอ่านรูปแบบตรวจสอบได้.
สรุปจากฝั่งผมในฐานะ Thomas Klein, MD: อาหารสำหรับไตที่ดีที่สุดคืออาหารที่ช่วยปรับ “ตัวบ่งชี้ที่เสี่ยง” ที่คุณมีอยู่จริง โดยไม่สร้างตัวใหม่ขึ้นมา หากโพแทสเซียมของคุณปกติ อย่ากลัวผักทุกชนิด หากค่า ACR ของคุณสูง ให้ให้ความสำคัญกับโซเดียมและความดันโลหิตอย่างจริงจัง หากฟอสเฟตเริ่มสูงขึ้น ให้ตามหาสารเติมแต่งก่อนจะตัดอาหารที่มีคุณค่าทั้งหมด และใช้ เครื่องวิเคราะห์เลือด AI Kantesti เพื่อติดตามรูปแบบตามเวลา.
คำถามที่พบบ่อย
อาหารที่ดีที่สุดสำหรับโรคไตคืออะไร โดยอิงจากผลตรวจเลือด?
อาหารที่ดีที่สุดสำหรับโรคไตขึ้นอยู่กับค่า eGFR, ACR ในปัสสาวะ, โพแทสเซียม, ฟอสฟอรัส, ไบคาร์บอเนต, ความดันโลหิต, สถานะโรคเบาหวาน และยาที่ใช้ โดยผู้ที่มี eGFR 72 มล./นาที/1.73 ตร.ม. และ ACR 250 มก./ก. อาจได้รับประโยชน์มากที่สุดจากการลดโซเดียมและการควบคุมความดันโลหิต ขณะที่ผู้ที่มี eGFR 28 และโพแทสเซียม 5.8 มิลลิโมล/ลิตร อาจจำเป็นต้องจำกัดโพแทสเซียม เป้าหมายโปรตีนก็แตกต่างกันเช่นกัน: แผน CKD ที่ยังไม่ต้องฟอกไตซึ่งมีการดูแลโดยผู้เชี่ยวชาญอาจใช้ประมาณ 0.55–0.8 ก./กก./วัน ในขณะที่ผู้ป่วยที่ฟอกไตมักต้องการประมาณ 1.0–1.2 ก./กก./วัน.
การปรับเปลี่ยนอาหารสามารถช่วยให้ค่า eGFR ดีขึ้นได้หรือไม่?
โดยทั่วไป อาหารไม่ได้ทำให้ค่า eGFR ที่แท้จริงเพิ่มขึ้นอย่างมากภายในไม่กี่วัน แต่สามารถช่วยปรับตัวชี้วัดความเสี่ยงรอบ ๆ ค่า eGFR ได้ การลดโซเดียมสามารถช่วยลดความดันโลหิตและอัลบูมินในปัสสาวะ การหลีกเลี่ยงภาวะขาดน้ำสามารถทำให้ค่าแครีเอตินินที่สูงเกินจริงกลับมาเป็นปกติได้ และการลดโปรตีนที่มากเกินไปสามารถช่วยลดค่า BUN ได้ หากค่า eGFR เพิ่มขึ้นหลังจากหยุดการออกกำลังกายหนัก ก่อนการตรวจที่มีการกินเนื้อสุกหรือใช้ครีเอทีน อาจสะท้อนถึงการวัดที่แม่นยำขึ้นมากกว่าเป็นการซ่อมแซมเนื้อเยื่อไต.
ผู้ที่เป็นโรคไตทุกคนควรหลีกเลี่ยงอาหารที่มีโพแทสเซียมสูงหรือไม่?
ไม่ อาหารที่มีโพแทสเซียมสูงไม่ควรถูกห้ามโดยอัตโนมัติในทุกคนที่มีโรคไต โพแทสเซียมโดยปกติมีช่วงประมาณ 3.5–5.0 mmol/L และการจำกัดจะมีความเกี่ยวข้องมากที่สุดเมื่อโพแทสเซียมสูงซ้ำ ๆ ประมาณ 5.0–5.5 mmol/L, eGFR ต่ำ หรือยาบางชนิด เช่น ACE inhibitors, ARBs หรือ spironolactone เพิ่มความเสี่ยงของโพแทสเซียม โพแทสเซียมจากอาหารทั้งส่วน เช่น ผลไม้และผัก ไม่ได้เหมือนกับสารทดแทนเกลือโพแทสเซียมคลอไรด์ ซึ่งอาจทำให้โพแทสเซียมสูงขึ้นอย่างรวดเร็ว.
ทำไมค่า BUN ของฉันถึงสูงขึ้นหลังจากกินโปรตีนมากขึ้น?
BUN จะสูงขึ้นเมื่อร่างกายสร้างยูเรียมากขึ้นจากการเผาผลาญโปรตีน ดังนั้นอาหารที่มีโปรตีนสูงอาจทำให้ BUN สูงขึ้นได้โดยที่ครีเอตินินไม่เพิ่มขึ้นในสัดส่วนเท่ากัน โดยทั่วไปค่า BUN ในผู้ใหญ่จะอยู่ราว 7–20 mg/dL แม้ว่าช่วงอ้างอิงจะแตกต่างกันตามแต่ละห้องปฏิบัติการ อัตราส่วน BUN ต่อครีเอตินินที่สูงกว่า 20:1 มักบ่งชี้ถึงภาวะขาดน้ำ การได้รับโปรตีนสูง ภาระไนโตรเจนจากทางเดินอาหาร หรือการไหลเวียนเลือดไปยังไตลดลง มากกว่าที่จะเป็นการเกิดแผลเป็นที่ไตเพียงอย่างเดียว.
อาหาร DASH ปลอดภัยสำหรับโรคไตหรือไม่?
อาหาร DASH อาจช่วยได้ในโรคไตเมื่อความดันโลหิตสูง แต่อาจต้องมีการปรับเปลี่ยนหากมีระดับโพแทสเซียมหรือฟอสฟอรัสสูง การทดลอง DASH-Sodium ดั้งเดิมพบว่าความดันโลหิตซิสโตลิกลดลงประมาณ 7.1 มม.ปรอทในผู้ใหญ่ที่ไม่เป็นความดันโลหิตสูง และลดลง 11.5 มม.ปรอทในผู้ใหญ่ที่เป็นความดันโลหิตสูง เมื่อรับประทานอาหารแบบ DASH ร่วมกับการจำกัดโซเดียม ในโรคไตเรื้อรังระยะที่ 4 หรือภาวะโพแทสเซียมสูงซ้ำๆ อาหาร DASH ที่มีโพแทสเซียมสูงตามมาตรฐานอาจต้องเปลี่ยนเป็นตัวเลือกที่มีโพแทสเซียมต่ำกว่า.
อาหารที่มีฟอสฟอรัสชนิดใดสำคัญที่สุดสำหรับผลตรวจการทำงานของไต?
สารเติมแต่งฟอสฟอรัสมักมีความสำคัญมากกว่าฟอสฟอรัสตามธรรมชาติในถั่ว เมล็ดพืช หรือธัญพืชเต็มเมล็ด เพราะฟอสฟอรัสที่เติมอาจถูกดูดซึมได้ที่ 90–100% โดยทั่วไประดับฟอสฟอรัสในเลือด (serum phosphorus) มักอยู่ในช่วง 2.5–4.5 มก./ดล. แต่ PTH อาจเพิ่มขึ้นก่อนที่ฟอสฟอรัสจะผิดปกติ ผู้ป่วยโรคไตเรื้อรัง (CKD) ควรตรวจดูคำที่เป็นส่วนประกอบซึ่งมีคำว่า “phos” บนฉลากอาหารบรรจุภัณฑ์ก่อนที่จะตัดโปรตีนจากพืชที่มีคุณค่าทางโภชนาการทั้งหมดออก.
ผลตรวจการทำงานของไตควรถือว่าเร่งด่วนเมื่อใด?
ผลตรวจทางห้องปฏิบัติการที่เกี่ยวกับไตอาจเป็นเรื่องเร่งด่วนเมื่อระดับโพแทสเซียมอยู่ที่ 6.0 mmol/L ขึ้นไป, ครีเอตินินเพิ่มขึ้นอย่างรวดเร็ว, โซเดียมต่ำมาก, ค่า CO2 ต่ำอย่างรุนแรง หรือมีอาการเช่น เจ็บหน้าอก เป็นลม สับสน อ่อนแรงมาก หรือหายใจลำบาก การที่ครีเอตินินเพิ่มขึ้น 0.3 mg/dL ภายใน 48 ชั่วโมงอาจเข้าเกณฑ์ภาวะไตบาดเจ็บเฉียบพลันได้ในสถานการณ์ที่เหมาะสม การปรับอาหารไม่ควรใช้เป็นคำตอบเพียงอย่างเดียวสำหรับผลตรวจไตหรือเกลือแร่ที่วิกฤต.
รับการวิเคราะห์ผลตรวจเลือดด้วย AI วันนี้
เข้าร่วมผู้ใช้งานมากกว่า 2 ล้านคนทั่วโลกที่ไว้วางใจ Kantesti สำหรับการวิเคราะห์ผลตรวจทางห้องแล็บแบบทันทีและแม่นยำ อัปโหลดผลตรวจเลือดของคุณ แล้วรับการอ่านผลตรวจเลือดอย่างครอบคลุมของไบโอมาร์กเกอร์ 15,000+ ภายในไม่กี่วินาที.
📚 งานวิจัยที่อ้างอิง
Klein, T., Mitchell, S., & Weber, H. (2026). กรอบการตรวจสอบความถูกต้องทางคลินิก เวอร์ชัน 2.0 (หน้า Medical Validation).
Klein, T., Mitchell, S., & Weber, H. (2026). AI วิเคราะห์ผลเลือด: วิเคราะห์ 2.5M การตรวจ | รายงานสุขภาพโลก 2026.
📖 อ้างอิงทางการแพทย์ภายนอก
KDIGO CKD Work Group (2024). KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney International.
📖 อ่านต่อ
สำรวจคู่มือทางการแพทย์ที่ผ่านการตรวจสอบโดยผู้เชี่ยวชาญเพิ่มเติมจาก คันเตสตี ทีมแพทย์:

อาหารสำหรับไขมันพอกตับ: เลือกอาหารแบบไหนที่ช่วยให้ผลตรวจดีขึ้น
การแปลผลโภชนาการสำหรับตับไขมัน อัปเดตปี 2026 สำหรับผู้ป่วยที่เข้าใจง่าย คู่มือปฏิบัติที่เน้นอาหารเป็นหลักเพื่อช่วยปรับแนวโน้มผลตรวจตับไขมัน...
อ่านบทความ →
อาหารเสริมชนิดใดที่ไม่ควรรับประทานร่วมกัน: คู่มือการจัดเวลา
การจัดเวลาอาหารเสริมและการแปลผลในห้องแล็บ อัปเดตปี 2026 สำหรับผู้ป่วย เข้าใจง่าย ปัญหาส่วนใหญ่ของอาหารเสริมไม่ใช่การปฏิสัมพันธ์ที่อันตราย แต่เป็นความผิดพลาดด้านเวลา...
อ่านบทความ →
แมกนีเซียมไกลซิเนต vs ซิเตรต: การนอนหลับ ความเครียด และผลตรวจเลือด
อัปเดตการแปลผลแล็บอาหารเสริมปี 2026 การตีความผลสำหรับผู้ป่วย Glycinate มักเหมาะกับเป้าหมายเรื่องการนอนหลับและความเครียด; citrate เป็นตัวเลือกที่เหมาะสมในทางปฏิบัติ...
อ่านบทความ →
การตรวจเลือดเพื่อภาวะเจริญพันธุ์: ฮอร์โมนที่คู่สมรสทั้งสองฝ่ายต้องมี
การแปลผลการตรวจฮอร์โมนเพื่อภาวะเจริญพันธุ์ อัปเดตปี 2026 สำหรับคู่รัก การตรวจเลือดที่มีประโยชน์ที่สุดสำหรับภาวะเจริญพันธุ์ ตรวจการตกไข่ สำรองรังไข่,...
อ่านบทความ →
การตรวจเลือดอะไรบ้างที่บอกปัญหาเกี่ยวกับหัวใจ? คู่มือเครื่องหมาย
การตีความผลตรวจตัวชี้วัดทางโรคหัวใจ อัปเดต 2026 การตรวจเลือดเพื่อหัวใจที่เป็นมิตรกับผู้ป่วยสามารถชี้ไปที่ภาวะหัวใจวาย ภาวะหัวใจล้มเหลว...
อ่านบทความ →
ฉันควรตรวจเลือดอะไรบ้างสำหรับอาการช้ำง่าย?
Easy Bruising Coagulation Labs อัปเดตปี 2026 สำหรับผู้ป่วย: คู่มือที่เป็นมิตรกับผู้ป่วย เน้นอาการก่อน—อาการอะไรบ้างที่มักตรวจดูจากรูปแบบผลแล็บเมื่อ...
อ่านบทความ →ค้นพบคู่มือสุขภาพทั้งหมดของเราและ เครื่องมือวิเคราะห์ผลตรวจเลือดที่ขับเคลื่อนด้วย AI ที่ kantesti.net
⚕️ ข้อสงวนสิทธิ์ทางการแพทย์
บทความนี้จัดทำเพื่อวัตถุประสงค์ด้านการศึกษาเท่านั้น และไม่ถือเป็นคำแนะนำทางการแพทย์ โปรดปรึกษาผู้ให้บริการด้านสุขภาพที่มีคุณสมบัติเหมาะสมเสมอสำหรับการตัดสินใจด้านการวินิจฉัยและการรักษา.
สัญญาณความน่าเชื่อถือ E-E-A-T
ประสบการณ์
การทบทวนเชิงคลินิกโดยแพทย์ที่นำโดยกระบวนการตีความผลตรวจในห้องแล็บ.
ความเชี่ยวชาญ
โฟกัสด้านเวชศาสตร์ห้องปฏิบัติการเกี่ยวกับพฤติกรรมของไบโอมาร์กเกอร์ในบริบททางคลินิก.
อำนาจ
เขียนโดย ดร. โธมัส ไคลน์ (Dr. Thomas Klein) พร้อมทบทวนโดย ดร. ซาราห์ มิตเชลล์ (Dr. Sarah Mitchell) และ ศ.ดร. ฮันส์ เวเบอร์ (Prof. Dr. Hans Weber).
ความน่าเชื่อถือ
การตีความที่อิงหลักฐาน พร้อมเส้นทางการติดตามที่ชัดเจนเพื่อลดความตื่นตระหนก.